Definen los parámetros hematológicos y moleculares para CCUS y el SMD
Por el equipo editorial de LabMedica en español
Actualizado el 11 May 2021
Los pacientes con citopenia clonal de significado indeterminado (CCUS, por sus siglas en inglés) tienen recuentos sanguíneos bajos y un examen de la médula ósea normal, pero las pruebas genéticas más avanzadas muestran la presencia de una mutación genética que probablemente cause los recuentos bajos.Actualizado el 11 May 2021
Los síndromes mielodisplásicos (SMD) son trastornos clonales de células madre hematopoyéticas, afecciones que pueden ocurrir cuando las células productoras de sangre en la médula ósea se vuelven anormales. Esto conduce a un bajo número de uno o más tipos de células sanguíneas. El SMD es considerado como un tipo de cáncer.
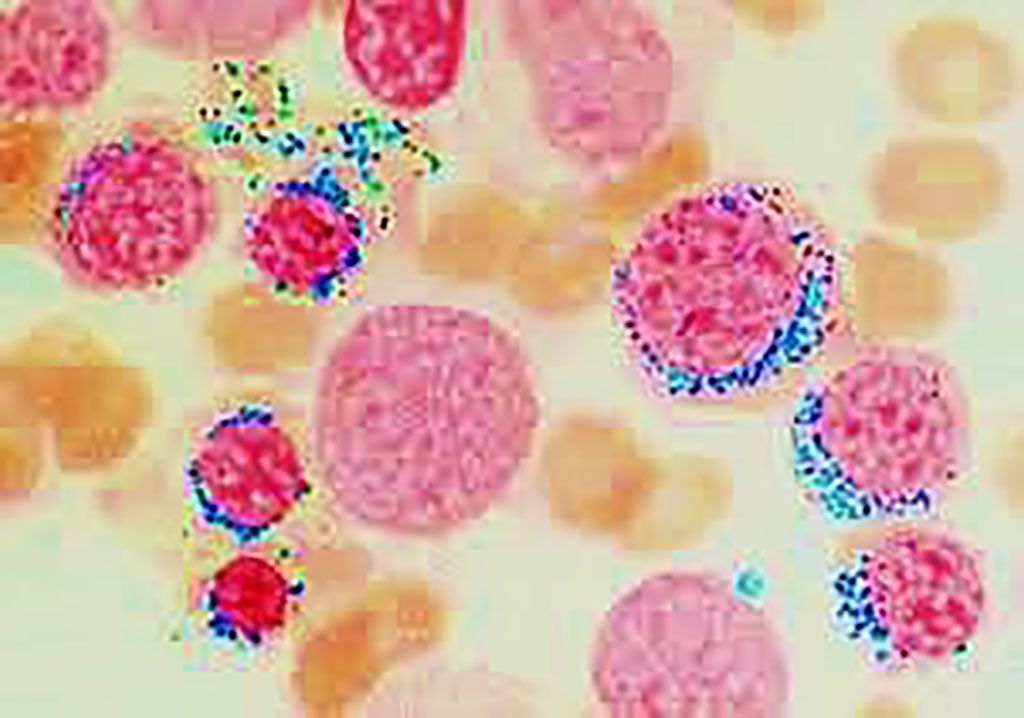
Imagen: Frotis de médula ósea de un paciente con anemia refractaria (SMD) con sideroblastos en anillo. La apariencia clásica de los sideroblastos anulares muestra la deposición de hierro en un “collar” alrededor del núcleo usando la coloración de Perls (Fotografía cortesía de la Universidad de Pavía)
Los hematólogos de la Clínica Mayo (Rochester, MN, EUA) y sus colegas, incluyeron en un estudio a un total de 187 pacientes: 75 (40%) con CCUS y 112 (60%) con SMD de menor riesgo (LR-SMD), con una mediana de edad de 66 años (63% hombres). En el grupo CCUS, 59 (78%) pacientes tenían ≥1 mutación somática, ocho (11%) tenían sólo anomalías citogenéticas clonales y ocho (11%) pacientes tenían mutaciones somáticas y anomalías citogenéticas clonales. Sesenta y siete (92%) pacientes tenían ≥ 1 mutación somática, y 45 (61%) tenían> 1 mutación. Las mutaciones comunes en CCUS incluyeron TET2 (30%), SRSF2 (20%), DNMT3A (13%) y ASXL1 (11%) con 17 (23%) pacientes con dependencia de transfusión de glóbulos rojos (TD) y 10 (13%) con dependencia del trasplante de plaquetas en el momento del diagnóstico.
Los científicos informaron que, en comparación con los pacientes con CCUS, los pacientes con LR-SMD tenían más probabilidades de tener recuentos de glóbulos blancos (WBC) más altos, recuentos absolutos de neutrófilos (ANC) más altos, recuentos de plaquetas más altos, tener DT de glóbulos rojos, tener sideroblastos en anillo (RS) en la médula ósea, tener un porcentaje de blastos en la MO más alto y tener mutaciones en SF3B1, mientras que los pacientes con CCUS tenían más probabilidades de tener recuentos absolutos de monocitos (AMC) más altos. El equipo observó un recuento de leucocitos/recuentos de plaquetas y glóbulos blancos más altos en pacientes con SMD en comparación con los pacientes con CCUS, en gran parte debido al hecho de que el 50% de la cohorte de SMD estaba compuesta por pacientes con displasia de linaje único (SLD) con SMD-RS, donde la displasia se limita en gran medida al linaje eritroide, evitando el desarrollo y la maduración de granulocitos y megacariocitos.
Los autores concluyeron que sus datos, entre otros, han llevado a criterios de clasificación operativa para el diagnóstico de CCUS que incluyen la presencia de mutaciones somáticas relevantes de las células mieloides con una frecuencia de alelos variante (VAF) ≥20%, sin presencia de displasia manifiesta en la médula ósea (MO) (<10% de células displásicas). Instan encarecidamente a la comunidad académica a considerar la inclusión de CCUS, especialmente CCUS-HighVAF (≥20%), como un subtipo de SMD en la próxima iteración del sistema de clasificación de la OMS. El estudio fue publicado el 27 de abril de 2021 en la revista Blood Advances.
Enlace relacionado:
Clínica Mayo