Estudian la aloinmunización Rh en pacientes con talasemia transfundidos crónicamente
Por el equipo editorial de LabMedica en español
Actualizado el 03 Mar 2021
Los pacientes con talasemia grave suelen necesitar transfusiones crónicas de por vida para proporcionar glóbulos rojos normales y suprimir la eritropoyesis ineficaz del propio paciente. La exposición acumulada aumenta el riesgo de aloinmunización de glóbulos rojos y posteriores reacciones transfusionales hemolíticas retardadas (DHTR).Actualizado el 03 Mar 2021
La prevalencia de aloinmunización entre pacientes con talasemia varía de 3% a 42%, con la mayoría de los anticuerpos dirigidos contra el sistema Rh. El sistema del grupo sanguíneo Rh no solo es el más inmunogénico después del ABO, sino que es muy complejo con más de 50 antígenos definidos serológicamente y más de 500 alelos RHD y RHCE identificados.
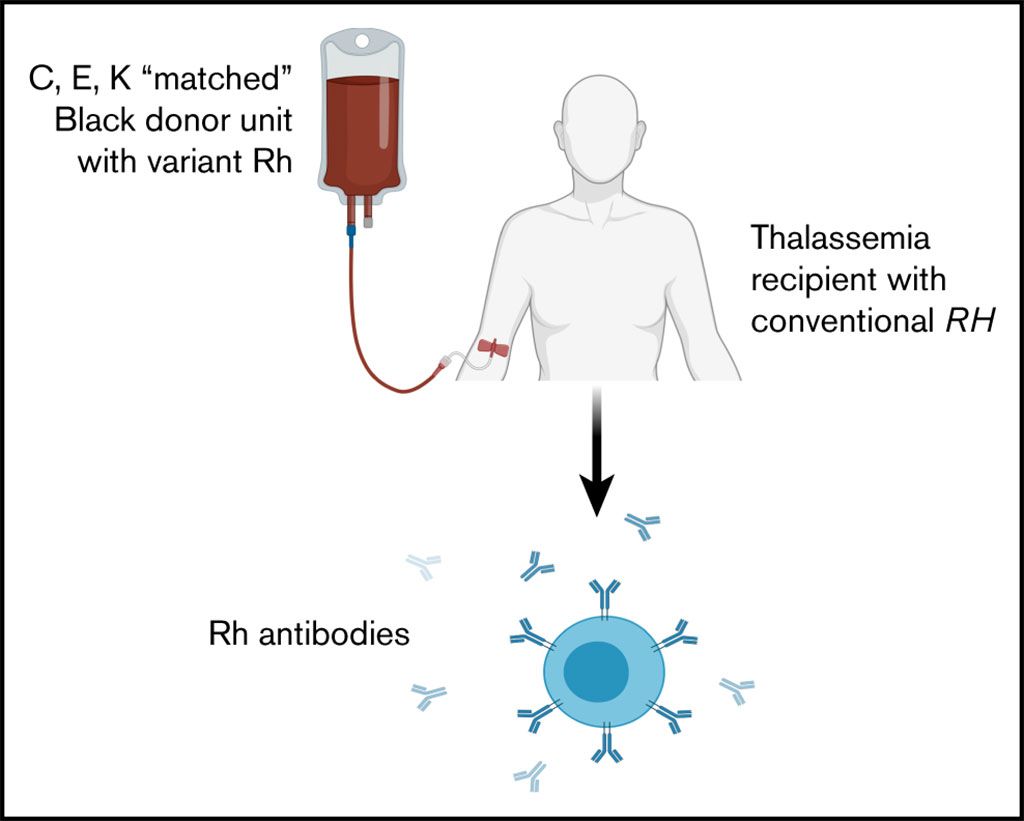
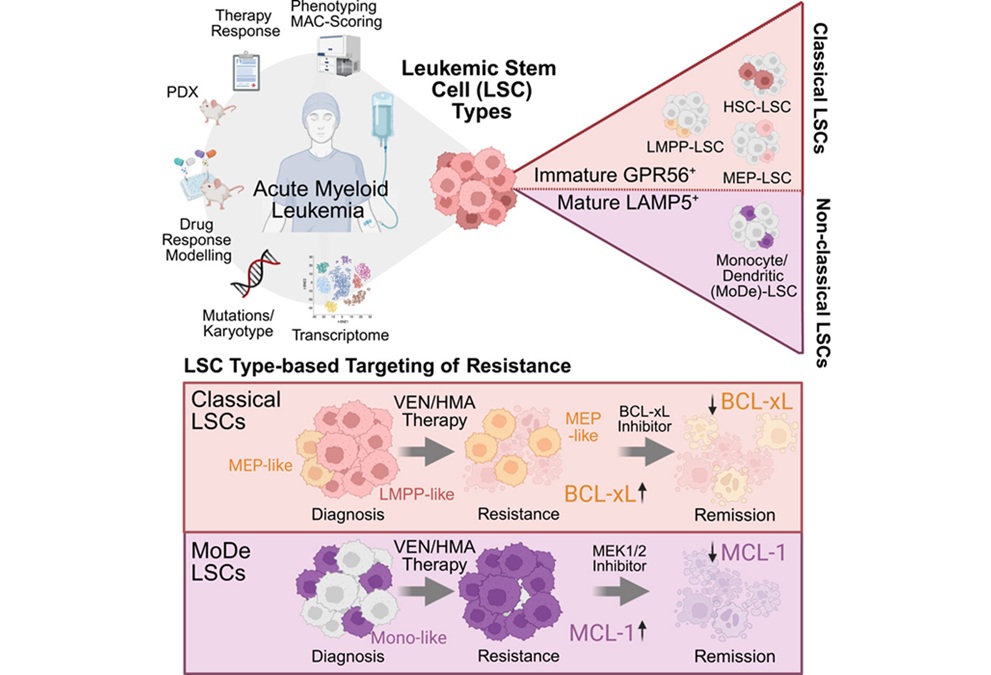
Imagen: Diagrama esquemático de la aloinmunización Rh en pacientes con transfusión crónica con talasemia, que reciben transfusiones compatibles con RhD, C, E y K (Fotografía cortesía del Hospital Infantil de Filadelfia).
Los científicos médicos del Hospital Infantil de Filadelfia (Filadelfia, PA, EUA), examinaron retrospectivamente los anticuerpos Rh entre 40 pacientes con transfusión crónica (asiáticos, blancos, afroamericanos, indios, del Medio Oriente) con talasemia, que recibieron una media de 174 Unidades de eritrocitos compatibles para los antígenos RhD, C, E y K profilácticas serológicas. Examinaron el genotipo Rh de los pacientes, así como la raza del donante y los fenotipos Rh durante tres eventos de transfusión anteriores a la detección de anticuerpos.
Se realizó un cribado de anticuerpos de tres células antes de cada transfusión o cuando se sospechaba un nuevo anticuerpo o DHTR. En 2003, la identificación de anticuerpos pasó del método del tubo a un método basado en gel (Ortho Clinical Diagnostics, Raritan, NJ, EUA). La tipificación del antígeno de glóbulos rojos se realizó mediante el método del tubo, pero a partir de 2017, obtuvieron los genotipos a través del BeadChip de Antígeno Eritrocitario Humano (Bioarray/Immucor, Warren, NJ, EUA). La genotipificación del factor Rh se realizó con las matrices RHD y RHCE BeadChip de Bioarray/Immucor y con ensayos basados en la reacción en cadena de la polimerasa.
Los investigadores detectaron 18 aloanticuerpos en 13 de 40 pacientes (32,5%), con una tasa de aloinmunización de 0,26 anticuerpos por 100 unidades transfundidas. Trece anticuerpos (72,2%) se dirigieron contra el factor Rh (cinco anti-D, cuatro anti-C, dos anti-E, uno anti-e y uno anti-V), a pesar de los fenotipos del donante que confirmaron la falta de transfusión de antígenos D, C o E, a pacientes que carecen de los antígenos correspondientes. Diez de 40 pacientes tenían un genotipo Rh alterado, pero los anticuerpos Rh no se asociaron con pacientes con Rh variante. Los donantes afroamericanos con una frecuencia conocida alta de variantes de Rh proporcionaron el 63% de las unidades transfundidas en las tres visitas anteriores a la detección inexplicable de anti-Rh.
Los autores concluyeron que la aloinmunización Rh no explicada por el genotipo Rh de los pacientes con talasemia o el fenotipo serológico de los donantes sugiere que se necesita una compatibilidad más precisa y que se debe explorar el papel de los genotipos Rh del donante en la aloinmunización. Extender el emparejamiento de Rh D, C y E para incluir c y e resultaría en unidades mejor emparejadas y minimizaría aún más la aloinmunización Rh. El estudio fue publicado el 2 de febrero de 2021 en la revista Blood Advances.
Enlace relacionado:
Hospital Infantil de Filadelfia
Bioarray/Immucor