Tecnología en miniatura mejora detección de enfermedades
Por el equipo editorial de LabMedica en español
Actualizado el 19 Jul 2017
Los investigadores han desarrollado una tecnología de impresión de microcontactos mejorada, para crear un dispositivo óptimo para el diagnóstico de enfermedades usando conjuntos de bioreceptores para los ensayos microfluidícos multiplexados.Actualizado el 19 Jul 2017
Dado que la eficiencia de los dispositivos de bioensayo microfluídicos, se basa en que los bioreceptores se encuentren tanto intactos como funcionales, la inmovilización de estos bioreceptores sin causar daños ha demostrado ser desalentadora. En las dos últimas décadas, se ha establecido la impresión con microcontactos, que utilizan un sello de goma para inmovilizar los bioreceptores, como un método robusto para crear una variedad de ensayos con múltiples aplicaciones. Sin embargo, este método también tiene sus defectos, particularmente cuando se utiliza en la escala nanométrica de las proteínas y el ADN. A esta escala, las técnicas utilizadas actualmente usan una resolución que no es la mejor, ya sea deformando el sello o dañando los bioreceptores, produciendo así datos bastante inmanejables para el diagnóstico u otras aplicaciones.
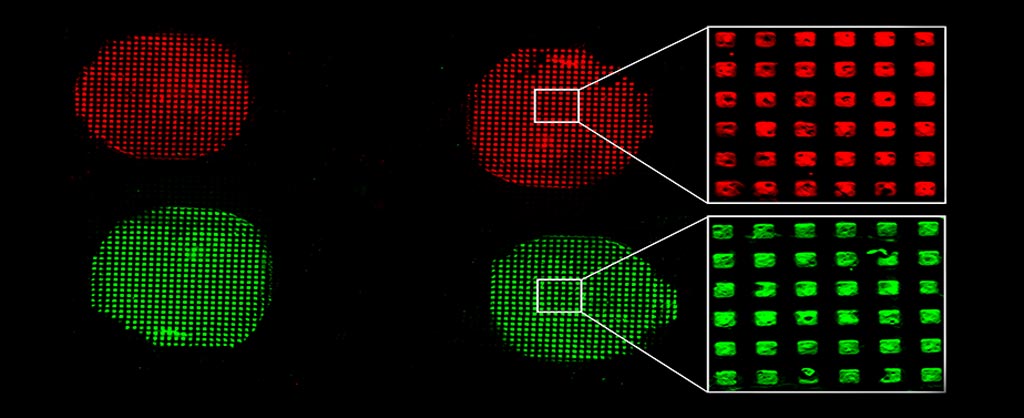
Imagen: Los dispositivos de bioensayo microfluídico son actualmente las herramientas de diagnóstico preferidas. Miden la concentración de biomarcadores de enfermedad contenidos en una muestra de un paciente, tal como la sangre, cuando pasa a través de una superficie que contiene bioreceptores inmovilizados para capturar el biomarcador. Pueden indicar la probabilidad de una enfermedad con base en la presencia/ausencia o sobre la base de la comparación de la concentración de biomarcadores en la muestra con relación al nivel normal del cuerpo (Imagen cortesía del Instituto de Ciencias y Tecnología de la Universidad de Posgrado de Okinawa).
Ahora, los investigadores en la Universidad de Posgrado y el Instituto de Ciencia y Tecnología de Okinawa (OIST, Okinawa, Japón) han desarrollado una secuencia de pasos de impresión que han solucionado estos problemas. Para la impresión de microcontactos “se necesita un sello, una tinta y una superficie, y luego se crea el patrón en la superficie. Es pan comido”, dijo el primer autor del artículo, Shivani Sathish, estudiante de doctorado en el OIST. El sello está hecho de polidimetilsiloxano (un sólido flexible similar al caucho utilizado en los sellos cotidianos), la tinta es (3-aminopropil) trietoxisilano (APTES, una solución compuesta de moléculas que contienen silicio y óxido), y la superficie es de vidrio.
Después de recubrir el sello con la tinta, el sello se presiona sobre el vidrio, y después, tras una incubación corta, se retira. El resultado es una capa modelada de APTES sobre el vidrio, un tablero de damas de regiones con o sin APTES. A continuación, se sella un dispositivo microfluídico (que contiene microcanales configurados para guiar el fluido a través de rutas especificadas) sobre el vidrio con los patrones. Finalmente, los bioreceptores se unen químicamente a las regiones con APTES dentro de los canales microfluídicos. El sistema está ahora listo para ser utilizado como un ensayo de diagnóstico, pasando una muestra de fluido corporal a través del dispositivo microfluídico unido al vidrio.
La solución APTES tiene una química conveniente. “Dependiendo de su bioreceptor de interés, sólo tiene que elegir la química adecuada para unir la molécula con el APTES”, dijo la señora Sathish. Se puede usar un sello para preparar un ensayo con la capacidad de inmovilizar una variedad de diferentes bioreceptores para multiplexación. Así, un sello permite múltiples pruebas y diagnósticos en una sola superficie. Esta característica sería ventajosa para el diagnóstico de enfermedades complejas como el cáncer, que se basa en pruebas que puedan detectar múltiples marcadores para mejorar el diagnóstico.
La Sra. Sathish y sus colegas hicieron patrones, inicialmente, de las características a nanoescala de la APTES usando tinta de APTES en agua, en contraposición a los productos químicos corrosivos, con lo que eliminaron el problema de hinchamiento de los sellos. Luego, inmovilizaron los bioreceptores sobre la superficie como la última etapa del proceso, después de hacer los patrones de APTES y fijar el dispositivo microfluídico. Al unir los bioreceptores como el paso final, los investigadores evitaron exponerlos a condiciones extremas y dañinas. Luego demostraron la eficacia del dispositivo final ejecutando un ensayo para capturar los biomarcadores interleuquina 6 y proteína C-reactiva humana, que, a menudo, se elevan durante la inflamación.
“El objetivo final es crear un dispositivo de punto de atención”, dijo la profesora del OIST, Amy Shen, que encabezó el estudio. “Si se pueden pre-inmovilizar los bioreceptores dentro de los dispositivos microfluídicos, se pueden utilizar como herramientas de diagnóstico cuando sea necesario”, continuó la señora Sathish, “Eventualmente, en lugar de tener un equipo clínico para procesar su muestra, esperamos que los pacientes mismos la puedan procesar en casa”.
El estudio fue publicado el 5 de abril de 2017 en la revista Analyst.