Células de órganos derivadas de iPS predicen sensibilidad a medicamentos
Por el equipo editorial de LabMedica en español
Actualizado el 04 May 2017
Actualizado el 04 May 2017
Al ensayar el medicamento pazopanib en células hepáticas derivadas de células madre específicas de pacientes, los investigadores han demostrado la primera prueba de concepto de un nuevo método que podría conducir al desarrollo de ensayos personalizados para determinar la toxicidad a los medicamentos en los pacientes.
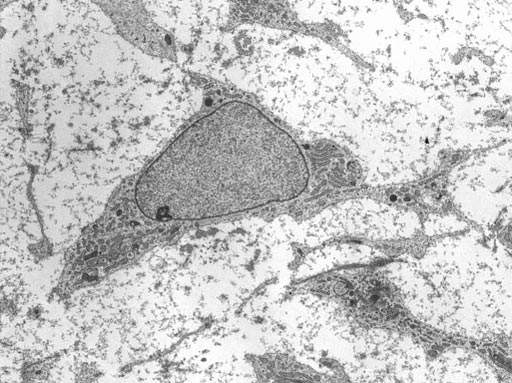
Imagen: Micrografía electrónica de transmisión (TEM) de una célula madre mesenquimal que presenta características ultraestructurales típicas (Fotografía cortesía de Robert M. Hunt).
Diferentes personas reaccionan de manera diferente al mismo medicamento, sin embargo, es difícil predecir los efectos secundarios de un individuo con antelación. Ahora, los investigadores del Instituto de Bioingeniería y Nanotecnología de Singapur (IBN) de A * STAR y el Centro Nacional de Cáncer de Singapur (NCCS) han desarrollado un método para detectar los efectos secundarios graves, mediante la primera prueba de un fármaco en células madre de la sangre del paciente.
“Los efectos secundarios adversos de los fármacos son una preocupación clínica importante, que podría y debería ser prevenible. Saber si un individuo es susceptible a un medicamento, en particular, mejorará la atención médica y el resultado del tratamiento”, dijo la profesora, Jackie Y. Ying, directora ejecutiva en el IBN.
En el estudio, los investigadores utilizaron células madre pluripotentes inducidas (iPS), para crear células similares al hígado, a partir de la sangre de cinco pacientes con cáncer de riñón. A continuación, las células del hígado fueron entonces expuestas al medicamento para el cáncer, pazopanib, que puede causar daño hepático. De los cinco pacientes: en tres se sabía que reaccionaban mal al pazopanib, mientras que en los otros dos no se presentaban efectos secundarios.
Los resultados mostraron que las células hepáticas derivadas de las iPS presentaban la misma sensibilidad al fármaco en comparación con sus datos posteriores al tratamiento procedentes de biopsias hepáticas. Utilizando estas células madre, los investigadores fueron capaces de analizar cómo el medicamento causaba el daño hepático, un mecanismo que era previamente desconocido.
El proyecto fue dirigido por el Dr. Min-Han Tan y el Prof. Hanry Yu del IBN. Los investigadores del NCCS reclutaron a los pacientes con cáncer de riñón y proporcionaron datos clínicos y análisis. “Nuestra hipótesis era que las células hepáticas hechas a partir de la sangre del individuo, podrían mostrar una sensibilidad o resistencia al pazopanib, similar a la presentada por el paciente. Este estudio es la primera prueba de concepto de que nuestro método puede predecir el daño hepático inducido por los medicamentos en un individuo. Es importante destacar que fuimos capaces de averiguar cómo funciona el medicamento por la forma en que reaccionan con las células del hígado”, dijo el Dr. Min-Han Tan. El Profesor Hanry Yu, añadió: “Actualmente, se están ensayando nuevos medicamentos, con respecto a la toxicidad, utilizando células hepáticas, genéricas, que no pueden modelar la reacción específica del paciente. A través de la personalización de las células del hígado de la sangre de los pacientes individuales, podemos ayudar a los médicos a formular terapias más seguras y más eficaces”.
“Estamos muy emocionados de que este estudio demuestre un método que podría transformar la forma en que se evalúa la toxicidad de los medicamentos. También arroja luz sobre el mecanismo de un efecto secundario particular del pazopanib, que puede conducir a maneras de superarlo. Ya estamos planeando ensayos clínicos formales sobre esto”, dijo el Dr. Ravindran Kanesvaran, consultor del NCCS.
Esta validación en pacientes sugiere que sería posible detectar células madre personalizadas que comprendan una serie de células hepáticas, pulmonares, renales y cardíacas, para predecir si el paciente tendría efectos secundarios por tomar un fármaco en particular. El equipo de investigación llevará a cabo más estudios sobre las drogas que afectan a otros tipos de órganos, y esperamos trabajar con los socios de la industria para hacer que esta tecnología esté ampliamente disponible.
El estudio fue publicado en la edición del 25 de enero de 2017 de la revista Scientific Reports.