Un chip de microfluidos sin patrones detecta marcadores del cáncer
Por el equipo editorial de LabMedica en español
Actualizado el 20 Mar 2019
El desempeño de los métodos microfluídicos actuales para la detección de exosomas está limitado por las condiciones de contorno, así como por los límites fundamentales para la transferencia de masas a microescala y la unión de los exosomas interfaciales.Actualizado el 20 Mar 2019
Algunos tipos de cáncer, como el cáncer de ovario, tienden a permanecer sin ser detectados hasta que están demasiado avanzados para que el tratamiento sea efectivo. Ahora, una herramienta innovadora puede ser capaz de detectar el cáncer de manera fácil, rápida y en cantidades minúsculas de sangre. Un dispositivo, que se llama “chip microfluídico con nanopatrones en 3D”, podría detectar con éxito los marcadores de cáncer en la gota más pequeña de sangre o en un componente de la sangre, llamado plasma.
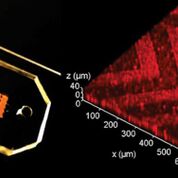
Imagen: El chip microfluídico tridimensional (3D) con nanopatrones en espiga que puede detectar el cáncer con más rapidez (Fotografía cortesía de la Universidad de Kansas).
Los bioquímicos de la Universidad de Kansas (Lawrence, KS, EU) y sus colegas, han demostrado que un chip microfluídico diseñado con nanopatrones en espiga tridimensionales autoensamblados, puede detectar niveles bajos de exosomas asociados con tumores en el plasma (10 exosomas μL−1, o aproximadamente 200 vesículas por 20 μL de muestra enriquecida) que de otro modo no serían detectables por los sistemas microfluídicos estándar por la biosensibilidad. Los nanopatrones promueven la transferencia de masa a microescala, aumentan el área de superficie y la densidad de la sonda para mejorar la eficiencia y la velocidad de la unión al exosoma, y permiten que el drenaje del líquido límite reduzca la resistencia hidrodinámica cerca de la superficie, promoviendo así las interacciones partícula-superficie para la unión del exosoma.
Los científicos utilizaron el dispositivo para la detección, en muestras de plasma de 2 μL de 20 pacientes con cáncer de ovario y de 10 controles pareados por edad, de subpoblaciones de exosomas que expresan CD24, la molécula de adhesión de células epiteliales y las proteínas alfa del receptor de folato. Sugieren el receptor alfa de folato exosómico como un biomarcador potencial para la detección temprana y la monitorización de la progresión del cáncer de ovario. El dispositivo con nanopatrones sin nanolitografía debe facilitar el uso de biopsias líquidas para el diagnóstico de cáncer.
Yong Zeng, PhD, profesor asociado de química y autor principal del estudio, dijo: “Históricamente, la gente pensaba que los exosomas eran como ‘bolsas de basura’ que las células podían usar para descargar contenidos celulares no deseados. Pero, en la última década, los científicos se dieron cuenta de que eran muy útiles para enviar mensajes a las células receptoras y comunicar información molecular importante en muchas funciones biológicas. Básicamente, los tumores envían exosomas que empaquetan moléculas activas que reflejan las características biológicas de las células parentales. Si bien todas las células producen exosomas, las células tumorales son realmente activas en comparación con las células normales”. El estudio se publicó el 25 de febrero de 2019 en la revista Nature Biomedical Engineering.
Enlace relacionado:
Universidad de Kansas





.jpg)