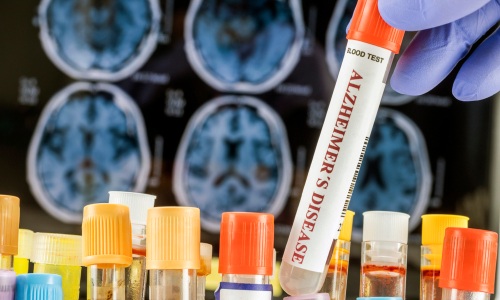
Aprueban sistema de monitorización de glucosa para unidades de cuidado crítico
Por el equipo editorial de LabMedica en español
Actualizado el 06 Nov 2014
Un sistema de monitorización de glucosa sanguínea (BGMS) ha sido aprobado y se ha extendido su uso a los pacientes con enfermedad crítica que han sido hospitalizados.Actualizado el 06 Nov 2014
Los usuarios de BGMS con las instrucciones de los fabricantes que no se pueden usar para los pacientes de los hospitales, críticamente enfermos, estarían sujetos a los requisitos de pruebas de alta complejidad bajo la Ley para el Mejoramiento de los Laboratorios Clínicos (CLIA), si tales sistemas fuesen a ser utilizados en la población hospitalaria en estado crítico. Estos requisitos incluyen la validación de lo bien que la BGMS funciona en esa población de pacientes.
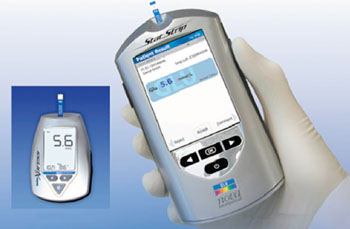
Imagen: El sistema hospitalario para la medición de glucosa StatStrip (Fotografía cortesía de Nova Biomedical).
La Dirección de Alimentos y Medicamentos de los EUA (FDA, Silver Springs, MD, EUA) determinó que el Sistema de Medición Hospitalario de Glucosa Nova StatStrip (Nova Biomedical, Waltham, MA, EUA) es fácil de usar y tiene un bajo riesgo de resultados falsos y le otorgó aprobación de estatus de prueba “exenta” bajo CLIA. Este estado exento les permitirá a una amplia variedad de profesionales de la salud, como enfermeras y técnicos, realizar la prueba en los puntos-de-atención, en lugar de exigir que se realice el examen en un laboratorio de un hospital u otro laboratorio que cumpla con los requisitos de la CLIA para las pruebas de alta complejidad. La exención CLIA también les permitirá a los laboratorios de los hospitales proporcionar, de forma segura la monitorización de la glucosa en sangre a los pacientes críticamente enfermos sin tener que cumplir los requisitos significativos de CLIA para las pruebas de alta complejidad.
Los datos que apoyan esta aprobación incluyeron un estudio de más de 1.650 pacientes con una variedad de condiciones médicas, que están tomando varios medicamentos, y son tratados en una variedad de departamentos del hospital, como las unidades cardiacas, de cuidados intensivos de emergencia y quirúrgicas. Los resultados mostraron concordancia con los resultados de glucosa en sangre que se compararon adecuadamente con los obtenidos con un analizador de glucosa en un laboratorio, en todos los tipos de pacientes evaluados. La aprobación es para indicaciones que incluyen el uso de sangre arterial o venosa total de los pacientes en todas las áreas de un hospital con varias condiciones, incluyendo: trauma, cáncer, sepsis e infección; problemas cardíacos, renales, neurológicos, obstetricia, ginecología, gastroenterología, endocrinos y de los pulmones; además de la gente se recupera de la cirugía general o cardiotorácica.
Enlaces relacionados:
Nova Biomedical
US Food and Drug Administration