Secuenciación fluorescente in situ ayuda a diagnosticar tejido enfermo
Por el equipo editorial de LabMedica en español
Actualizado el 14 Apr 2014
La secuenciación fluorescente in situ tiene aplicaciones potenciales como nuevos diagnósticos que detectan los signos más precoces de enfermedad.Actualizado el 14 Apr 2014
La secuenciación fluorescente in situ del ARN (FISSEQ), podría llevar a un diagnóstico anterior del cáncer, al revelar los cambios moleculares que conducen a cáncer en el tejido aparentemente sano. Puede seguir las mutaciones del cáncer y su respuesta a las terapias dirigidas modernas, y descubrir los objetivos para los tratamientos más seguros y eficaces. El método también podría ayudar a los biólogos a comprender cómo cambian sutilmente los tejidos durante el desarrollo embrionario e, incluso, ayudar a cartografiar el laberinto de las neuronas. Los investigadores describieron el método en la edición digital de febrero de 2014, de la revista Science.
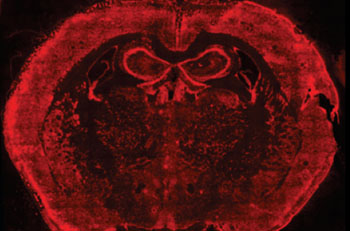
Imagen: Los ARNs están marcados de rojo en el cerebro del ratón (Fotografía cortesía de la Facultad de Medicina de Harvard y el Instituto Wyss).
El Instituto Wyss de Ingeniería Inspirada Biológicamente en la Universidad de Harvard y la Facultad de Medicina de Harvard (Boston, MA, EUA) en colaboración con el Instituto Allen para la Ciencia del Cerebro (Seattle, WA, EUA) desarrollaron el nuevo método que le permite a los científicos ubicar miles de ARNm y otros tipos de ARN en células intactas, mientras realizan la determinación de la secuencia de letras. Los ARN mensajeros (ARNm) se colocan a lo largo de los tejidos vivos, y su ubicación a menudo ayuda a regular la forma en que las células y los tejidos crecen y se desarrollan. Hasta hoy, con el fin de analizar muchos ARNm de forma simultánea, los científicos tenían que moler las células hasta una pulpa, algo que los deja sin un método para identificar su ubicación dentro de la célula.
“Al observar exhaustivamente la expresión de los genes dentro de las células, ahora podemos observar numerosas diferencias importantes en los tejidos complejos como el cerebro que son invisibles hoy”, dijo George Church, profesor de genética de la Facultad de Medicina de Harvard y miembro principal de la facultad en el Instituto Wyss. “Esto nos ayudará a entender como nunca antes cómo los tejidos se desarrollan y funcionan en la salud y en la enfermedad”.
Las células humanas sanas normalmente encienden alrededor de la mitad de sus 20.000 genes en cada momento, y eligen aquellos genes cuidadosamente para producir las respuestas celulares deseadas. Por otra parte, las células pueden marcar la expresión génica hacia arriba o hacia abajo, ajustando para producir desde unas pocas copias de trabajo de un gen a varios miles. El Prof. George Church y Je Hyuk Lee, un investigador de la Facultad de Medicina de Harvard y el Instituto Wyss, quisieron señalar la localización celular de los ARNm. Querían determinar simultáneamente la secuencia de estos ARNs, que los identifica y revela a menudo su función.
El equipo trató primero el tejido químicamente para fijar las miles de moléculas de ARN de las células en su lugar. Luego usaron enzimas para copiar esos ARNs en réplicas de ADN, y copiar esas réplicas muchas veces para crear una pequeña bola de réplica de ADN fijada al mismo sitio. Se las arreglaron para fijar y reproducir miles de los ARNs de la célula a la vez-pero entonces los ARNs estaban tan apretujada dentro de la célula que incluso un microscopio y la cámara, adaptados, no podían diferenciar las luces intermitentes de una bola individual de ADN réplica de aquellas de sus vecinos.
Para resolver ese problema los investigadores asignaron a la célula una dirección única: la secuencia de “letras” o bases, en la propia molécula de ARN. Se imaginaron que pudieran leer la dirección usando métodos similares a la secuenciación de ADN de próxima generación, un conjunto de métodos de secuenciación del genoma de alta velocidad que el Prof. Church ayudó a desarrollar a comienzos del siglo XXI.
Los científicos trataron de fijar el ARN en su lugar en la celda, haciendo una pequeña bola con muchas réplicas ADN coincidente de los ARN, y luego adaptaron la secuenciación de próxima generación del ADN, para que funcionara en células fijadas. Los cuatro colores intermitentes revelarían la secuencia de bases de cada réplica de ADN, lo que les diría la secuencia de bases del ARN correspondiente del que se derivaban. Y esas secuencias, en teoría, proporcionarían un número ilimitado de direcciones únicas-una para cada uno de los ARN originales.
El método, llamado secuenciación fluorescente in situ del ARN (FISSEQ), podría llevar a un diagnóstico anterior del cáncer, al revelar los cambios moleculares que conducen a cáncer en el tejido aparentemente sano. Puede realizar un seguimiento de las mutaciones del cáncer y cómo responder a las terapias dirigidas, modernas y descubrir los objetivos para tratamientos más seguros y eficaces.
Enlaces relacionados:
Allen Institute for Brain Science
Wyss Institute of Biologically Inspired Engineering at Harvard University and Harvard Medical School