Ensayos basados en IA respaldan la estratificación del riesgo en cáncer de próstata y de mama
Actualizado el 30 Apr 2026
Los cánceres de próstata y mama se encuentran entre las neoplasias malignas más diagnosticadas en todo el mundo, y la heterogeneidad de su biología dificulta la estratificación del riesgo y la selección del tratamiento. Los médicos buscan cada vez más herramientas objetivas que utilicen la patología de rutina para anticipar el riesgo de progresión e identificar a los pacientes con mayor probabilidad de beneficiarse de terapias complementarias.
Un nuevo conjunto de ensayos de inteligencia artificial (IA), con marcado CE, permite ahora realizar una evaluación de riesgo personalizada y brindar apoyo en la toma de decisiones terapéuticas para estos cánceres en toda Europa.
Artera ha obtenido lel marcado CE conforme al Reglamento Europeo de Diagnóstico In Vitro (EU IVDR) para sus pruebas ArteraAI para biopsia de próstata y ArteraAI para cáncer de mama. La prueba ArteraAI para biopsia de próstata, el producto insignia de la compañía, se posiciona como la primera prueba de diagnóstico in vitro con IA para el cáncer de próstata con marca CE en la Unión Europea. El ensayo estima la probabilidad de progresión de la enfermedad y el riesgo de mortalidad, y evalúa si es probable que los pacientes se beneficien de añadir terapia hormonal a corto plazo (ST-ADT) al tratamiento.
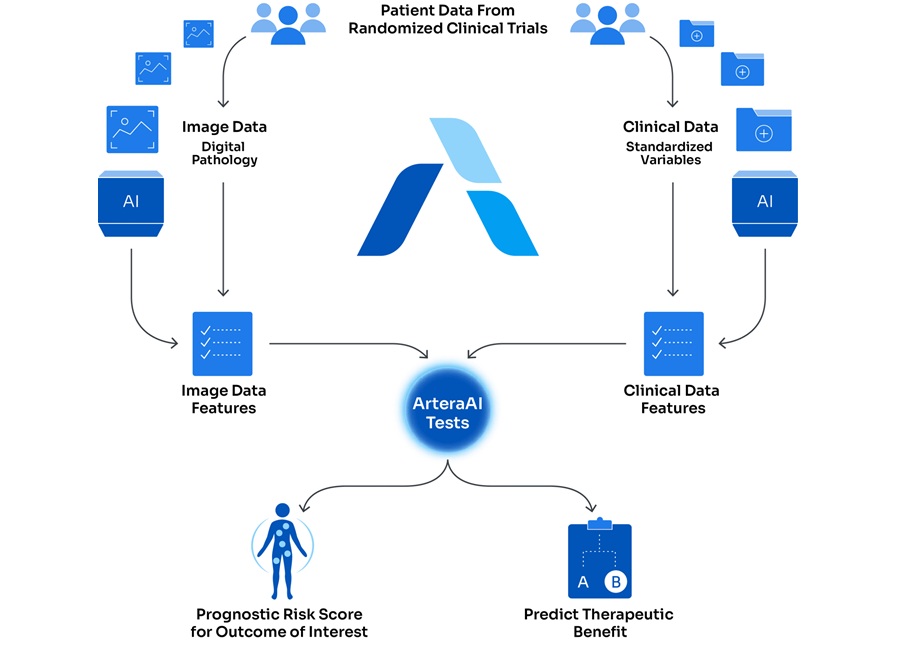
Ambos ensayos se basan en un enfoque de IA multimodal (MMAI) que analiza imágenes histopatológicas digitalizadas junto con variables clínicas del paciente para caracterizar la agresividad del tumor y el posible beneficio del tratamiento. El software está destinado a su uso por laboratorios de patología tras un diagnóstico de cáncer para proporcionar una estratificación de riesgo mejorada. Está diseñado para integrarse en los flujos de trabajo existentes del laboratorio sin requerir nuevos procedimientos.
El marcado CE permite el uso clínico en los 27 Estados miembros de la Unión Europea y en los países de la AELC, incluidos Islandia, Liechtenstein y Noruega, lo que en conjunto cubre una población de aproximadamente 450 millones de personas. Los ensayos fueron evaluados en cuanto a calidad, seguridad general y requisitos de desempeño, con evidencia clínica considerada aplicable.
Estas autorizaciones europeas siguen a la reciente autorización De Novo de la Administración de Alimentos y Medicamentos de EE. UU. (FDA) para ArteraAI Prostate, el primer software impulsado por IA autorizado para pronosticar resultados a largo plazo en pacientes con cáncer de próstata no metastásico.
Con la certificación CE para cáncer de próstata y de mama, Artera posiciona su plataforma entre las primeras soluciones de IA para múltiples tipos de cáncer disponibles en la Unión Europea. La plataforma MMAI ha sido validada clínicamente en cohortes de pacientes a nivel mundial y presentada en importantes foros científicos, incluido el Simposio de Cáncer de Mama de San Antonio. La compañía informa que mantiene conversaciones con laboratorios de patología y socios sanitarios en toda Europa para establecer vías locales de acceso y pedidos.
"La obtención de la marca CE para nuestras pruebas de cáncer de próstata y mama representa un hito fundamental para Artera y subraya la escalabilidad de nuestra plataforma de IA multimodal (MMAI)", declaró Andre Esteva, director ejecutivo y cofundador de Artera.
"La validación de nuestro enfoque basado en IA bajo uno de los marcos regulatorios más rigurosos del mundo marca un paso importante en nuestro despliegue global y avanza en nuestra misión de llevar la toma de decisiones impulsada por IA a la oncología de precisión".
Enlaces relacionados
Artera