Panel de biomarcadores con citoesponja prioriza la vigilancia endoscópica del esófago de Barrett
Actualizado el 17 Feb 2022
Se recomienda vigilancia endoscópica para pacientes con esófago de Barrett porque, aunque el riesgo de progresión es bajo, la intervención endoscópica es altamente efectiva para displasia de alto grado y cáncer. Sin embargo, la endoscopia repetida tiene daños asociados y el acceso ha sido limitado durante la pandemia de COVID-19. El objetivo fue evaluar el papel de un dispositivo no endoscópico (Cytosponge) junto con biomarcadores de laboratorio y factores clínicos para priorizar la endoscopia para el esófago de Barrett.
El esófago de Barrett es una lesión precancerosa que aumenta el riesgo de adenocarcinoma esofágico a través de etapas intermedias de aumento de la anomalía morfológica en la histología, descrita como esófago de Barrett no displásico, displasia de bajo grado, displasia de alto grado y adenocarcinoma invasivo.
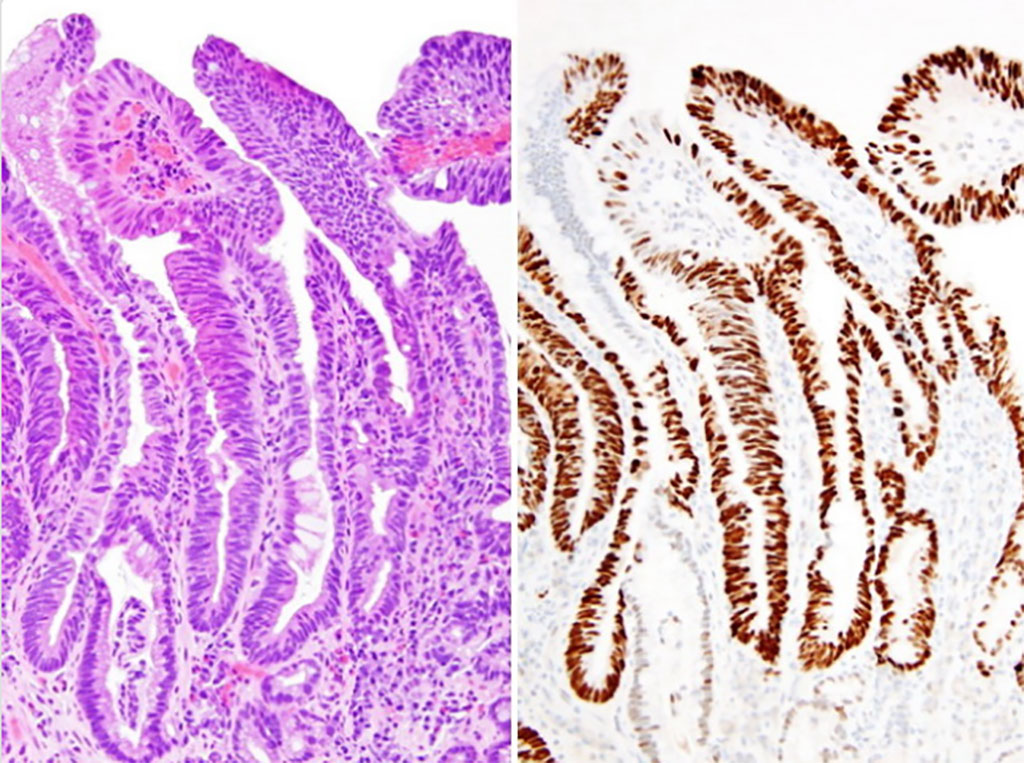
Se ha demostrado que un dispositivo de recolección de células esofágicas, no endoscópico, conocido como Cytosponge, junto con una prueba de biomarcadores para el factor de trébol 3 (TFF3), aumenta la detección del esófago de Barrett diez veces más que el estándar de atención actual. Como una extensión lógica de este hallazgo, se podrían aplicar biomarcadores adicionales a Cytosponge para identificar la displasia y el carcinoma.
Un gran equipo de científicos médicos de la Unidad de Cáncer MRC de la Universidad de Cambridge (Cambridge, Reino Unido), realizó un estudio retrospectivo, multicéntrico y transversal en pacientes mayores de 18 años que estaban en vigilancia endoscópica para esófago de Barrett, con metaplasia intestinal confirmada por TFF3 y longitud mínima del segmento de Barrett de 1 cm. Los participantes se dividieron en cohortes de entrenamiento (n=557) y validación (n=334) para identificar los grupos de riesgo óptimos.
Después de la recuperación, la Cytosponge se colocó en líquido conservante SurePath (TriPath Imaging, Burlington, NC, EUA) y se mantuvo a 4°C. Tanto la atipia como la inmunohistoquímica de p53 se realizaron en portaobjetos fijados en formol e incluidos en parafina de la Cytosponge. La atipia se evaluó en la lámina coloreadas con hematoxilina y eosina e incluyó displasia clara y atipia de significado desconocido. Una inmunohistoquímica p53 (Novocastra Laboratories, Newcastle, Reino Unido) en el sistema de coloración automática BondMax, con el kit de detección de polímeros Leica Bond (Leica Biosystems, Milton Keynes, Reino Unido), con una intensidad de la coloración de 3 se consideró significativa.
Los investigadores informaron que la prevalencia de displasia de alto grado o cáncer, determinada por el estándar de oro actual de biopsia endoscópica fue del 17 % (92/557 pacientes) en la cohorte de entrenamiento y del 10 % (35/344) en la cohorte de validación. A partir del nuevo análisis de biomarcadores, se identificaron tres grupos de riesgo: alto riesgo, definido como atipia o expresión exagerada de p53 o ambas en la muestra con Cytosponge; riesgo moderado, definido por la presencia de un factor de riesgo clínico (edad, sexo y longitud del segmento) y bajo riesgo, definido como Cytosponge negativa y sin factores de riesgo clínico.
El riesgo de displasia de alto grado o cáncer intramucoso en el grupo de alto riesgo fue del 52 % (68/132 pacientes) en la cohorte de entrenamiento y del 41 % (31/75) en la cohorte de validación, en comparación con el 2 % (5/210 pacientes), y 1% (2/185) en el grupo de bajo riesgo, respectivamente. En el entorno del mundo real, los resultados de la Cytosponge identificaron prospectivamente a 39/223 (17 %) pacientes como de alto riesgo (atipia o expresión exagerada de p53, o ambos) que requerían endoscopia, entre los cuales el valor predictivo positivo fue del 31 % (12/39 pacientes) para displasia de alto grado o cáncer intramucoso y 44 % (17/39) para cualquier grado de displasia.
Los autores concluyeron que se podría usar la atipia en las Cytosponges, la expresión exagerada de p53 y los factores de riesgo clínicos (edad, sexo y longitud del segmento), para priorizar a los pacientes para la endoscopia. La investigación adicional podría validar su uso en la práctica clínica y dar lugar a una reducción sustancial de los procedimientos de endoscopia en comparación con las vías de vigilancia actuales. El estudio fue publicado el 1 de febrero de 2022 en la revista The Lancet Oncology.
Related Links:
Unidad de Cáncer MRC
TriPath Imaging
Novocastra Laboratories
Leica Biosystems