Evalúan un análisis de biopsia líquida para la detección precoz del cáncer gástrico
Por el equipo editorial de LabMedica en español
Actualizado el 14 Sep 2021
El cáncer gástrico (CG) es el cuarto cáncer más comúnmente diagnosticado y la tercera causa principal de mortalidad asociada al cáncer en todo el mundo. A pesar de las mejoras en las modalidades de tratamiento, el pronóstico del CG avanzado después de la resección curativa permanece malo.Actualizado el 14 Sep 2021
Los pacientes diagnosticados con CG en estadio temprano tienen un pronóstico favorable, lo que subraya el paradigma de que la identificación en estadios tempranos sigue siendo una estrategia atractiva para reducir la mortalidad de los pacientes, asociada al CG. El uso de biomarcadores de cáncer no invasivos basados en biopsias líquidas se ha vuelto cada vez más deseable, y se han identificado varios biomarcadores moleculares prometedores en sangre, orina y jugo gástrico.
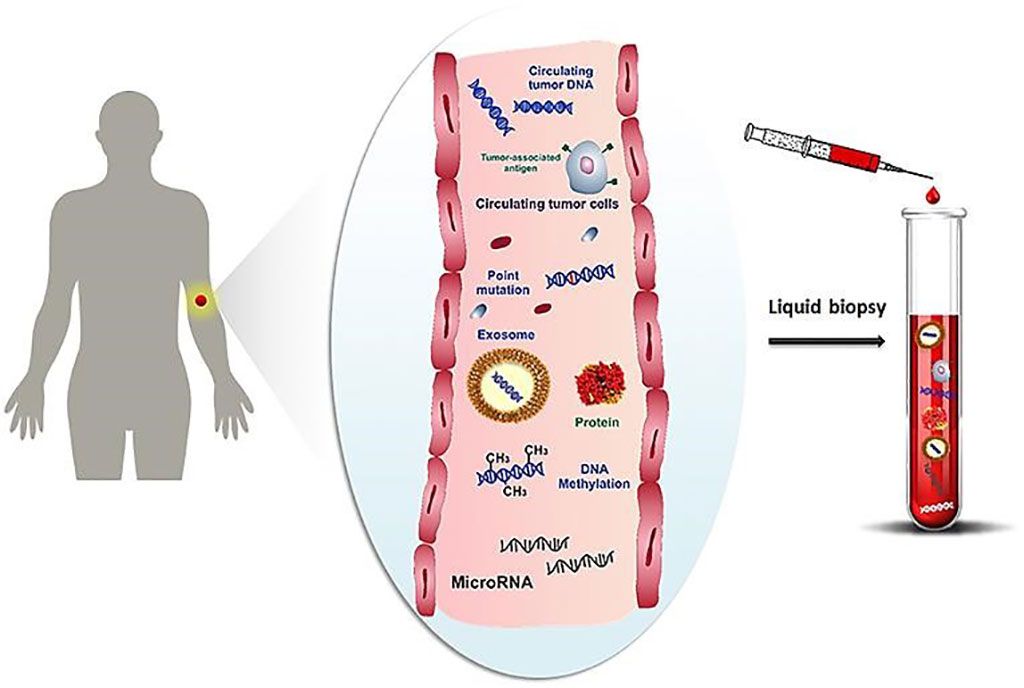
Imagen: Representación esquemática de biomoléculas relacionadas con el cáncer, como células, proteínas, ácidos nucleicos, miARN y microvesículas que circulan en el torrente sanguíneo y recolección de estos biomarcadores mediante biopsia líquida (Fotografía cortesía de la Universidad de Florencia)
Los gastroenterólogos del Centro Médico de la Universidad Baylor (Dallas, TX) y sus colegas internacionales, analizaron más de 1.900 muestras de tejido y suero de pacientes con CG, tejidos normales adyacentes y participantes sanos en cuatro fases. Las fases del estudio incluyeron una fase de descubrimiento de biomarcadores, una fase de validación de tejidos, una fase de validación retrospectiva del suero y una fase prospectiva de evaluación del desempeño del suero.
Se analizó la cohorte de descubrimiento de biomarcadores (436 tejidos CG y 41 mucosas normales adyacentes) para identificar candidatos a miARN. En la fase de validación de tejidos, se realizaron ensayos cuantitativos de reacción en cadena de la polimerasa con transcripción inversa (qRT-PCR) para interrogar los niveles de expresión de los miARN candidatos en 50 pares de tumores primarios y adyacentes, recién congelados, coincidentes y tejidos normales adyacentes de pacientes con CG. En la fase de validación prospectiva del suero, se recolectaron muestras de suero de 176 pacientes con CG y 173 participantes sanos, emparejados por edad y sexo, que fueron reclutados prospectivamente desde marzo de 2017 hasta agosto de 2018. Los 10 miARN se validaron en dos conjuntos de datos independientes adicionales que incluyeron 40 muestras de CG y 40 de tejido no canceroso con datos de perfiles de miARN adquiridos mediante el microarray de miARN (Agilent Technologies, Santa Clara, CA, EUA).
Los científicos informaron que los conjuntos de datos para la etapa de análisis de perfiles de expresión de todo el genoma incluían 598 muestras totales de pacientes (284 [55,4%] de hombres; edad media ± SE del paciente, 65,7 ± 0,5 años). La firma de 10 miARN resultante se validó en dos cohortes de suero retrospectivas de pacientes con CG (586 pacientes; 348 [59,4%] hombres, edad media ± SE, 66,0 ± 0,7 años), lo que llevó al establecimiento de una firma de 5 miARN (AUC, 0,90) que también mostró altos niveles de desempeño diagnóstico en pacientes con enfermedad en estadio I (AUC, 0,89) Se derivó un modelo de puntuación de riesgo y el ensayo se optimizó para un número mínimo de miARN. A continuación, se validó el desempeño de la firma de 3-miARN resultante en una cohorte prospectiva de 349 pacientes con CG.
La firma final de 3-miARN (miR-18a, miR-181b y miR-335) mostró una alta exactitud diagnóstica en todos los estadios de los pacientes (AUC, 0,86), incluso en pacientes con enfermedad en estadio I (AUC, 0,85). Esta firma de miARN fue superior a los marcadores sanguíneos utilizados actualmente y superó al cribado endoscópico en un análisis de costo-efectividad (índice de costo-efectividad incremental [2.304,80 dólares por año de vida ajustado por calidad]).
Los autores concluyeron que su estudio estableció una firma de miARN circulante robusta, no invasiva para la detección de CG, y validó su potencial diagnóstico en múltiples cohortes de pacientes independientes, tanto retrospectivas como prospectivas, destacando su posible aplicación para la detección temprana de pacientes con CG. El estudio fue publicado el 24 de agosto de 2021 en la revista JAMA Network Open.
Enlace relacionado:
Centro Médico de la Universidad Baylor