Demuestran aplicaciones de la ERM para la recurrencia del cáncer con un análisis del ADNc
Por el equipo editorial de LabMedica en español
Actualizado el 22 Jul 2020
El ADN tumoral circulante (ADNc) se encuentra en el torrente sanguíneo y se refiere al ADN que proviene de células cancerosas y tumores. La mayor parte del ADN está dentro del núcleo de una célula. A medida que crece un tumor, las células mueren y son reemplazadas por otras nuevas. Las células muertas se descomponen y su contenido, incluido el ADN, se libera al torrente sanguíneo.Actualizado el 22 Jul 2020
Las tasas de recurrencia del cáncer varían ampliamente entre los tipos de cáncer y dentro de los tipos de cáncer según el estadio, la histología, los factores genéticos, los factores relacionados con el paciente y los tratamientos. Enfermedad residual mínima (ERM) es el nombre dado a un pequeño número de células leucémicas (células cancerosas de la médula ósea) que permanecen en la persona durante el tratamiento o después del tratamiento cuando el paciente está en remisión (sin síntomas ni signos de enfermedad). Es la principal causa de recaída en el cáncer y la leucemia.
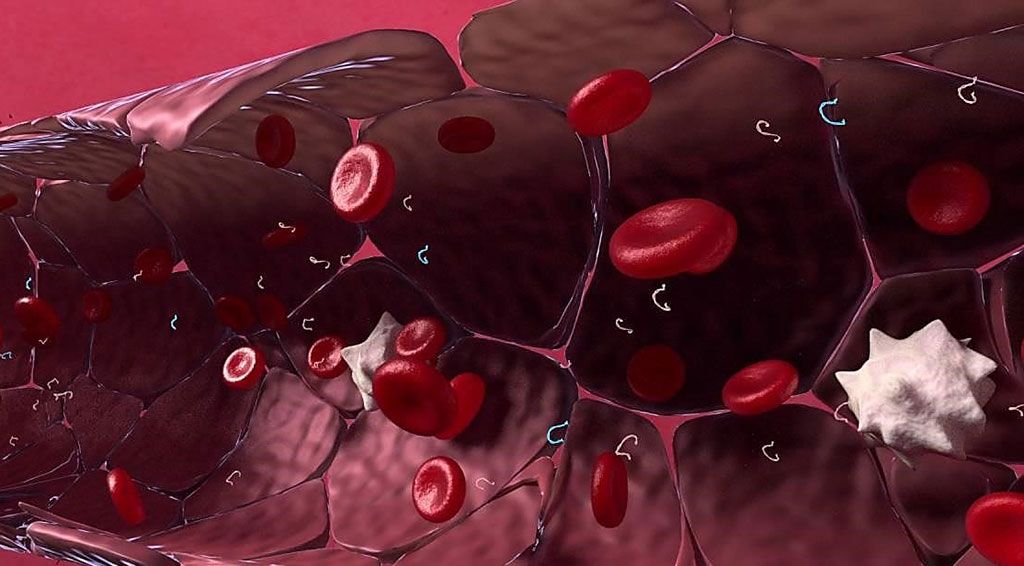
Imagen: El ensayo RaDaR (enfermedad residual y recurrencia) detecta el ADN tumoral circulante (ADNc) que se encuentra en el torrente sanguíneo (Fotografía cortesía de Inivata).
Los científicos del Instituto de Investigación del Cáncer UK Cambridge (Cambridge, Reino Unido) analizaron tres líneas celulares de cáncer a diferentes diluciones, material de referencia de ADN, siete muestras incluidas en parafina y fijadas en formalina (de mama, colon y melanoma), así como 366 muestras de cáncer de pulmón del estudio de ADN tumoral circulante de cáncer de pulmón (LUCID). Utilizaron entradas de ADN de 20.000 o 4.000 copias.
El equipo utilizó el ensayo RaDaR (enfermedad residual y recurrencia) (Inivata, Babraham, Reino Unido). El ensayo RaDaR específico para pacientes de Inivata se ejecuta en la plataforma de secuenciación InVision de la compañía, que se basa en una tecnología llamada secuenciación de amplicones específicos. RaDaR analiza el tumor de un paciente de una cirugía de resección y puede señalar hasta 48 mutaciones únicas en el cáncer del paciente. Después de realizar la secuenciación del exoma completo (WES) en el tejido tumoral de un paciente para identificar variantes somáticas, Inivata clasifica y prioriza las variantes basadas en algoritmos patentados para diseñar un panel específico para cada paciente.
Los investigadores que usaron 48 mutaciones encontraron que RaDaR tenía una sensibilidad del 97% con el uso de 20.000 copias, y del 63% con 4.000 copias a una dilución variante de 20 partes por millón (equivalente a una frecuencia de alelo variante de 0,002%), con una especificidad del 100%. Al observar un subconjunto de 16 mutaciones, RaDaR produjo una sensibilidad del 97% a 40 partes por millón, 75% a 20 partes por millón y 38% a 10 partes por millón, también con un 100% de especificidad. Los colegas del equipo realizaron un segundo estudio y evaluaron el valor pronóstico de RaDaR y su capacidad para detectar ADNc antes o durante la recaída, en pacientes con cáncer de pulmón de células no pequeñas (CPCNP) en estadio I a estadio III, tratados con intención curativa con un éxito similar.
Karen Howarth, DPhil, directora de genómica del cáncer en Inivata y coautora de los estudios, dijo: “Si estás poniendo 10.000 copias en una reacción y buscas una molécula mutante, ves una molécula en un fondo de 10.000. Pero, si lo divides en cuatro muestras usando partición, solo debes ver una molécula en 2.500 moléculas, lo que aumenta la señal”. Los estudios se presentaron en el congreso virtual 2020 de la Asociación Americana para la Investigación del Cáncer celebrado del 22 al 24 de junio de 2020.
Enlace relacionado:
Instituto de Investigación del Cáncer UK Cambridge
Inivata