Citometría de masas con imágenes descubre subgrupos novedosos de cáncer de mama
Por el equipo editorial de LabMedica en español
Actualizado el 04 Feb 2020
Cambiar el curso de cómo se tratan y curan finalmente las enfermedades requiere una comprensión integral de los fenotipos celulares complejos y sus interrelaciones en el contexto espacial del microambiente tisular.Actualizado el 04 Feb 2020
Los análisis unicelulares han revelado una gran heterogeneidad entre y dentro de los tumores humanos, pero los fenotipos complejos de una sola célula y su contexto espacial no se reflejan actualmente en la estratificación histológica que es la base de muchas decisiones clínicas.

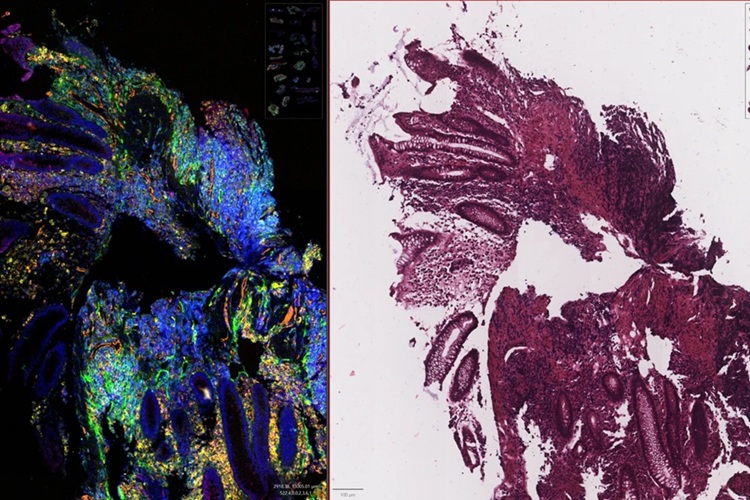
Imagen: El Sistema de Imagenología Hyperion trae una tecnología CyTOF demostrada junto con la capacidad de obtener imágenes para potenciar la detección simultánea de cuatro a 37 marcadores de proteínas usando la citometría de masa con imágenes (Fotografía cortesía de Fluidigm).
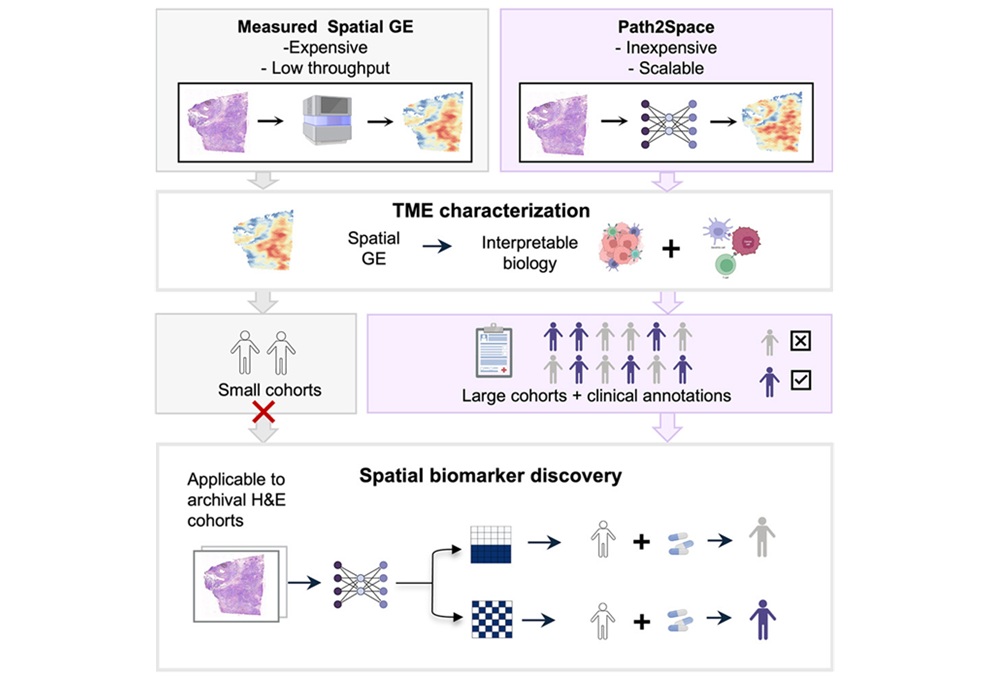
Los científicos de la Universidad de Zúrich (Zúrich, Suiza) y sus colegas, utilizaron la citometría de masas con imágenes para cuantificar simultáneamente 35 biomarcadores, obteniendo 720 imágenes de patología de alta dimensión de tejido tumoral de 352 pacientes con cáncer de mama, con una supervivencia a largo plazo disponible para 281 pacientes. El equipo concentró sus esfuerzos en células individuales dentro de estas imágenes para perfilar profundamente los fenotipos y la organización de los tumores.
Los investigadores utilizaron el Sistema de imágenes Hyperion (Fluidigm, South San Francisco, CA, EUA) que combina la coloración inmunohistoquímica con la detección basada en espectrometría de masas para generar imágenes. Para su análisis, diseñaron un panel de citometría de masas con imágenes de cáncer de mama específico de 35 anticuerpos, incluidos los destinados a detectar objetivos establecidos como el receptor de estrógenos, el receptor de progesterona y HER2, pero también el marcador de proliferación Ki-67 y los marcadores de linaje celular. El equipo informó que sus imágenes eran comparables a las generadas mediante métodos de inmunohistoquímica o inmunofluorescencia.
Al cuantificar la expresión de estos marcadores, el equipo pudo evaluar las características espaciales de estas células individuales y colocarlas en clústeres de fenotipos, de los que identificaron 14 principales. Además, descubrieron 18 subgrupos de patología unicelular. Estos subgrupos, observaron, diferían de los subtipos clínicos clásicos y estaban asociados con resultados clínicos distintos. Por ejemplo, el subgrupo 1 de patología unicelular (SCP1) se asoció con pacientes con un pronóstico prometedor, mientras que SCP3 se relacionó con un pronóstico peor.
Cuando compararon subtipos clínicamente definidos y subgrupos de patología unicelular, los científicos descubrieron que el enfoque basado en células individuales era más capaz de predecir la supervivencia general de un paciente. Repitieron su análisis en un conjunto de muestras tumorales de 73 pacientes y del mismo modo descubrieron los mismos metaclústers celulares y subgrupos de patología unicelular. Sin embargo, notaron una diferencia en la proporción de los subgrupos presentes, que atribuyeron a las diferencias en las estrategias de selección de pacientes para las dos cohortes.
Chris Linthwaite, MBA, presidente y director ejecutivo de Fluidigm, dijo: “Este estudio histórico es el primero en demostrar el valor clínico potencial de la citometría de masas por imágenes altamente multiplexada para identificar subtipos de cáncer de seno que se correlacionan con los resultados clínicos. Al arrojar nueva luz con imágenes espaciales unicelulares y datos sobre las características del microambiente tumoral, creemos que este estudio aumentará aún más la adopción de la IMC en investigaciones traslacionales y clínicas para ofrecer mejores métodos predictivos y personalizados para la atención del cáncer en el futuro”. El estudio fue publicado el 20 de enero de 2020 en la revista Nature.
Enlace relacionado:
Universidad de Zúrich
Fluidigm