Una prueba en sangre predice el rechazo del trasplante de riñón
Por el equipo editorial de LabMedica en español
Actualizado el 20 Mar 2019
Un trasplante renal ofrece el mejor tratamiento para los pacientes cuyos riñones han fallado; en el Reino Unido se realizan aproximadamente 3.000 cada año. El rechazo agudo ocurre cuando el sistema inmunológico del cuerpo comienza a atacar el órgano donado.Actualizado el 20 Mar 2019
Este rechazo es una complicación común en el primer año después de realizado el trasplante, afectando a aproximadamente dos de cada 10 pacientes. Puede afectar la vida útil del órgano trasplantado. En la actualidad, solamente se puede confirmar el rechazo agudo mediante una biopsia del órgano trasplantado. Si bien el rechazo agudo se puede tratar, esto solo se puede hacer cuando el órgano ya está afectado y ya se ha producido el daño.
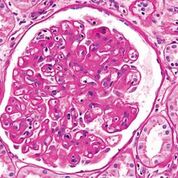
Imagen: Fotomicrografía de un glomérulo con cambios característicos de una glomerulopatía por trasplante. La glomerulopatía por trasplante se considera una forma de rechazo crónico mediado por anticuerpos (Fotografía cortesía de Nephron).
Los científicos de la Fundación NSH de Guy's y St Thomas (Londres, Reino Unido) y sus colegas, recolectaron muestras de sangre en serie de 455 receptores consecutivos de trasplantes de riñón (KTR, por sus siglas en inglés), trasplantados en un solo centro regional de trasplantes. Las muestras se recolectaron en 26 puntos temporales durante las consultas clínicas realizadas durante el primer año posterior al trasplante. Un total de 1.464 muestras de 248 pacientes fueron utilizadas en el estudio, incluyendo 66 pacientes con un episodio de rechazo.
El equipo examinó la expresión cuantitativa de la reacción en cadena de la polimerasa de transcripción inversa (RT-qPCR) de 22 genes basados en la literatura en las muestras de sangre periférica de 248 pacientes. Para seleccionar los genes, utilizaron una regresión logística penalizada basada en 27 pacientes estables y 27 que hicieron rechazo, demostrada por biopsia, mediado por células T, que cumplían con estrictos criterios de inclusión/exclusión. Validaron esta firma en un grupo independiente de pacientes estables y pacientes con células T concomitantes y rechazo mediado por anticuerpos; pacientes de un estudio independiente; y muestras de pre-biopsia transversales de pacientes que no hicieron rechazo, y muestras de seguimiento longitudinales que cubren el primer año posterior al trasplante de los rechazadores, los no rechazadores y los pacientes estables.
Usando estas muestras y analizando los datos a lo largo del tiempo, desarrollaron una combinación característica de siete genes que diferenciaron a los pacientes que desarrollaron el rechazo de los que no lo hicieron. Una firma parsimoniosa de rechazo mediado por células T (TCMR, por sus siglas en inglés) (IFNG, IP-10, ITGA4, MARCH8, RORc, SEMA7A y WDR40A) mostró un área bajo la curva ROC validada de forma cruzada de 0,84. El equipo también identificó una firma de seis genes para una forma menos común de complicación. La nefropatía por virus BK puede parecer clínicamente similar al rechazo agudo, pero requiere una terapia muy diferente, que reduce la inmunosupresión. Ser capaz de poder diferenciar entre estas complicaciones significaría que los médicos puedan garantizar que los pacientes reciban el tratamiento más adecuado.
Los autores concluyeron que las alteraciones de los marcadores moleculares en la sangre emergen mucho antes del TCMR clínicamente manifiesto. La monitorización de una firma TCMR en sangre periférica podría desentrañar la actividad proinflamatoria relacionada con las células T y los procesos inmunológicos ocultos. Esta información adicional podría respaldar las decisiones de manejo clínico en pacientes con función renal estable pero deficiente o con resultados de biopsia no concluyentes.
Paramit Chowdhury, MD, PhD, nefrólogo consultor y autor principal del estudio, dijo: “Este avance podría marcar una gran diferencia en nuestra capacidad para monitorizar a los pacientes de trasplante de riñón y tratar el rechazo con anterioridad. También puede salvar a algunos pacientes de una biopsia innecesaria. Es un primer paso para obtener una mejor comprensión del estado del sistema inmunológico de un paciente, permitiendo una mejor adaptación del tratamiento antirechazo del paciente”. El estudio se publicó el 1 de marzo de 2019 en la revista EBioMedicine.
Enlace relacionado:
Fundación NSH de Guy's y St Thomas