Evalúan el uso de pruebas rápidas seriadas de antígeno del SARS-CoV-2 durante los brotes
Por el equipo editorial de LabMedica en español
Actualizado el 02 Aug 2021
Las pruebas seriadas en las instalaciones para el SARS-CoV-2 pueden ayudar a identificar casos en entornos de brotes, lo que permite la implementación rápida de precauciones basadas en la transmisión y estrategias de prevención y control de infecciones.Actualizado el 02 Aug 2021
Aunque las pruebas de reacción en cadena de la polimerasa con transcripción inversa en tiempo real (RT-PCR) realizadas en un laboratorio tienen la mayor sensibilidad, su tiempo de respuesta prolongado puede retrasar la implementación de la cuarentena y el aislamiento. Las pruebas de antígenos son fáciles de usar y producen resultados en minutos, lo que facilita una acción rápida, especialmente durante los brotes en entornos colectivos.
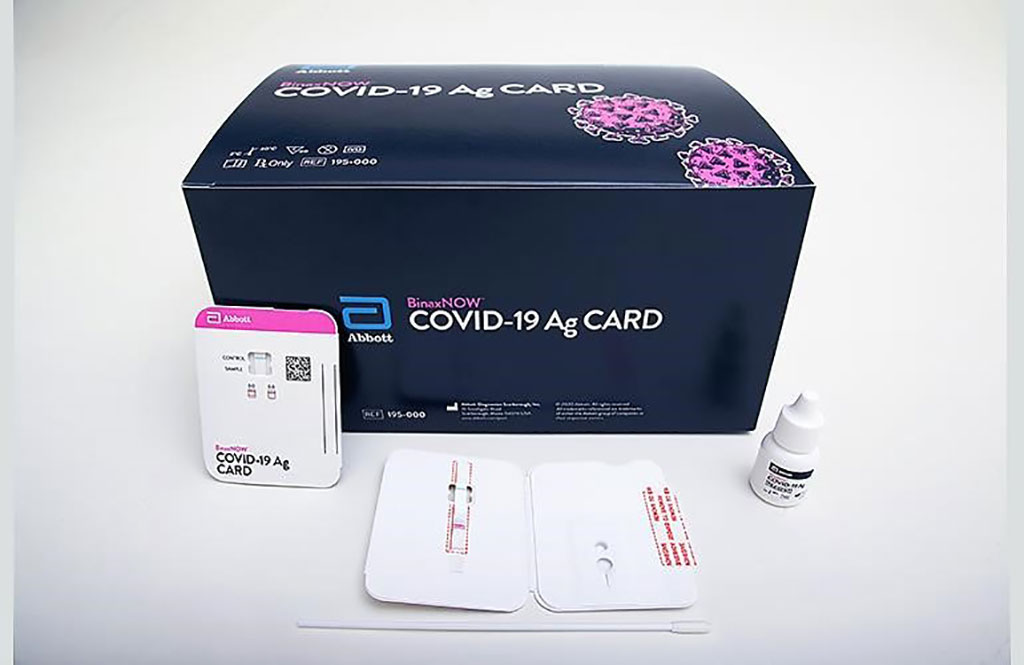
Imagen: Tarjetas Ag BinaxNOW COVID-19 (Fotografía cortesía de Abbott Laboratories)
Los científicos médicos de los Centros para el Control y la Prevención de Enfermedades (CDC, Atlanta, GA, EUA), llevaron a cabo un estudio prospectivo que incluyó 532 muestras de 234 residentes disponibles y personal en un hogar de ancianos que experimentaron un brote de SARS-CoV-2 para evaluar el desempeño de la prueba de antígenos cuando se utiliza durante un brote emergente. Se recolectaron dos muestras de todos los residentes y del personal tres veces durante un período de 13 días. Científicos de laboratorio capacitados analizaron un hisopo in situ utilizando una prueba rápida de antígenos y el otro se envió a los CDC para realizar pruebas de referencia de cultivo de virus y RT-PCR.
Se comparó el porcentaje de concordancia positiva (PPA) y el porcentaje de concordancia negativa (PNA) para las tarjetas BinaxNOW COVID-19 Ag (Abbott Laboratories, Abbott Park, IL, EUA) con la prueba de RT-PCR utilizando el Análisis Multiplex CDC Influenza SARS-CoV-2 (Flu SC2) en el instrumento de PCR en tiempo real Applied Biosystems 7500 Fast Dx (Thermo Fisher Scientific, Waltham, MA, EUA) y el cultivo del virus se realizó utilizando células Vero CCL-81.
El equipo informó que la prueba BinaxNOW PPA con cultivo de virus, utilizada para la detección de virus con capacidad de replicación, fue del 95%. Sin embargo, la PPA general de las pruebas de antígenos con RT-PCR fue del 69% y la APN fue del 98%. Cuando solo se analizó el primer resultado positivo de la prueba para cada participante, la PPA de la prueba de antígeno con RT-PCR fue del 82% entre 45 personas sintomáticas y del 52% entre 343 personas asintomáticas. En comparación con la RT-PCR y el cultivo de virus, la prueba BinaxNOW se comportó bien en la infección temprana (86% y 95%, respectivamente) y mal en la infección tardía (51% y sin recuperación de virus, respectivamente).
Los autores concluyeron que, aunque sus datos sugieren que casi un tercio de las infecciones positivas a RT-PCR se pasaron por alto en total, la prueba de antígeno pudo identificar el 86% de las infecciones cuando las pruebas se realizaron durante la infección temprana, cuando las personas tienen más probabilidades de ser infecciosas. Trabajos anteriores han demostrado que las personas pueden continuar dando positivo en la prueba del SARS-CoV-2 mediante RT-PCR durante semanas después de que ya no sean infecciosas. Por lo tanto, las comparaciones de las pruebas de antígenos con cultivos de virus podrían proporcionar una medida más exacta del desempeño de las pruebas de antígenos para identificar personas infecciosas. El estudio fue publicado el 27 de abril de 2021 en la revista Annals of Internal Medicine.
Enlace relacionado:
Centers for Disease Control and Prevention
Thermo Fisher Scientific