Se detecta el patógeno de la úlcera de Buruli mediante un análisis isotérmico RPA
Por el equipo editorial de LabMedica en español
Actualizado el 04 Mar 2019
La úlcera de Buruli (UB) es una enfermedad tropical desatendida causada por Mycobacterium ulcerans. La patogénesis de la UB está relacionada con la producción de una toxina policétida conocida como micolactona, que es citotóxica y tiene propiedades inmunomoduladoras; la enfermedad se presenta como nódulos, placas, úlceras y edema.Actualizado el 04 Mar 2019
La amplificación de ácidos nucleicos de la secuencia de inserción IS2404, por la reacción en cadena de la polimerasa (PCR), es el método más sensible y específico para detectar M. ulcerans, el agente causal de la UB. Sin embargo, la PCR no siempre está disponible en comunidades endémicas en África debido a su costo y sofisticación tecnológica. La microscopía para los bacilos con la coloración de Ziehl-Neelsen y el cultivo para M. ulcerans tienen baja sensibilidad y la histopatología es un examen que rara vez está disponible en las áreas endémicas.
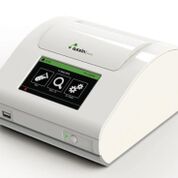
Imagen: El Instrumento de Diagnóstico Isotérmico T8 proporciona resultados cuantitativos y cualitativos para aplicaciones de ensayos isotérmicos de diagnóstico molecular (Fotografía cortesía de Axxin).
Un equipo de científicos asociados con la Universidad de Ciencia y Tecnología Kwame Nkrumah (Kumasi, Ghana) evaluó el desempeño clínico del ensayo para M. ulcerans (Mu-RPA) utilizando ADN extraído de aspirados con aguja fina o de frotis tomados de 67 pacientes en los que se sospechaba una UB y de 12 pacientes con lesiones no UB, confirmadas clínicamente. El equipo desarrolló un sistema de amplificación isotérmica de ADN utilizando el método de amplificación de la polimerasa recombinasa (RPA).
Todas las muestras se analizaron con la PCR en tiempo real y con el ensayo Mu-RPA para determinar la sensibilidad clínica y la especificidad del ensayo utilizando la PCR en tiempo real como la prueba de referencia. En el caso de la detección con la RPA en tiempo real, se utilizó el kit TwistAmp Exo de “Formulación Mejorada” (TwistDX Ltd, Cambridge, Reino Unido). Se midió la detección de fluorescencia a 570 nm para el canal FAM y se estableció un umbral al aumentar la fluorescencia por encima de las tres desviaciones estándar sobre el fondo detectado en el primer minuto de incubación. El equipo programó el fluorómetro T8 utilizando la aplicación de Escritorio T8-ISO (Axxin Pty Ltd, Fairfield, Australia) con el fin de poder detectar las diluciones más bajas que cumplían con los criterios para diferenciar las muestras positivas de los controles negativos con base en diluciones en serie del estándar molecular.
Los científicos analizaron todas las muestras utilizando los ensayos RPA y PCR en tiempo real y 58 de estas muestras fueron confirmadas por PCR como UB. De los 58 casos confirmados, 51 se identificaron correctamente mediante el ensayo de RPA con siete resultados falsos negativos con una sensibilidad del 88%. Las 21 muestras de PCR negativas fueron todas negativas por RPA, especificidad del 100% y un valor predictivo positivo (PPV) del 100% con un índice de Youden del 88%. Cuando el análisis se estratificó por tipo de muestra, la sensibilidad y la especificidad de la RPA para los hisopos en comparación con la PCR fueron del 92% y 100%, respectivamente, con un VPP del 100%. Del mismo modo, la sensibilidad y especificidad de las muestras de aspirados de aguja fina fueron 82% y 100% respectivamente.
Los autores concluyeron que el ensayo de RPA en tiempo real, desarrollado para la detección rápida y exacta del ADN de M. ulcerans tiene alta sensibilidad, especificidad y reproducibilidad y es comparable a la PCR en tiempo real. El ensayo fue significativamente más rápido que los métodos de PCR en tiempo real disponibles para detectar M. ulcerans con un tiempo de ejecución de 15 minutos, en comparación con casi dos horas para la PCR en tiempo real. Potencialmente, la prueba Mu-RPA se puede utilizar en un entorno de bajos recursos más cercano a los pacientes cuando se combina con un método rápido de extracción de ADN. El estudio fue publicado el 1 de febrero de 2019 en la revista PLOS NTD.
Enlace relacionado:
Universidad de Ciencia y Tecnología Kwame Nkrumah
TwistDX
Axxin Pty Ltd