Nuevos análisis moleculares detectan virus del papiloma humano
Por el equipo editorial de LabMedica en español
Actualizado el 23 Apr 2009
Se han presentado dos análisis moleculares nuevos en los Estados Unidos para la detección del virus del papiloma humano (VPH). La prueba de alto riesgo está diseñada para detectar los 14 tipos de alto riesgo del VPH que se saben, causan cáncer de cuello uterino, mientras que el análisis 16/18 es una prueba para genotipificar los tipos de VPH 16 y 18, que están asociados con aproximadamente el 70% de los cánceres de cuello uterino en los Estados Unidos.Actualizado el 23 Apr 2009
La Administración de Alimentos y Drogas de los Estados Unidos (FDA; Rockville, MD, EUA) ha dado la aprobación de venta de dos análisis de Hologic (Bedford, MA, EUA), Cervista HPV alto riesgo (AR) y Cervista HPV 16/18, para análisis del VPH. Esto significa que Hologic es la segunda firma en obtener aprobación para vender un diagnóstico molecular para el cáncer de cuello uterino, en los Estados Unidos.
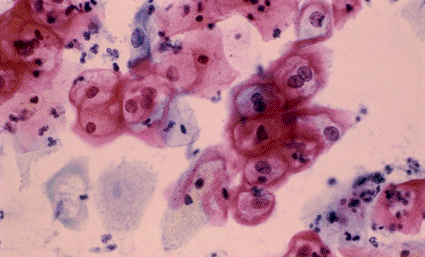
Imagen: Microfotografía de luz de un frotis de cuello uterino que muestra células epiteliales infectadas con el virus del papiloma humano (VPH) (Fotografía cortesía de SPL).
La prueba Cervista HPV AR incluye un control interno para verificar la celularidad adecuada para análisis, lo cual debería reducir el potencial de resultados falsos negativos. La compañía también observó que requiere un volumen de muestra más pequeño que pude minimizar los resultados no concluyentes o indeterminados, lo cual debería reducir la necesidad de llamar nuevamente a las pacientes para repetir los exámenes. Las cepas de VPH identificadas mediante la prueba Cervista HPV-16/18 representan los dos tipos más oncogénicos y persistentes de VPH.
"Creemos, que aunque la competencia está creciendo, el mercado del VPH es significativamente grande y con poca penetración, permitiendo que varios participantes tengan éxito”, escribió Peter Lawson, un analista en Thomas Weisel Partners (San Francisco, CA, EUA), una firma especializada en segmentos en crecimiento de la economía. "El mercado de los Estados Unidos ha sido penetrado en apenas un 25%, mientras que la penetración en Europa y Asia está en un solo dígito”. El factor más importante para el mercado ocurriría si la prueba de VPH reemplaza a la citología cervico-uterina como la prueba primaria, lo cual debería suceder en los países europeos más pequeños en el futuro cercano, aunque la adopción amplia todavía está a muchos años”.
Enlaces relacionados:
US Food and Drug Administration
Hologic
Thomas Weisel Partners