Herramienta de patología digital con IA para la estratificación del riesgo en cáncer de mama
Actualizado el 15 May 2026
La evaluación del riesgo en el momento del diagnóstico es fundamental para guiar el tratamiento del cáncer de mama invasivo en estadio temprano, con receptor hormonal positivo y receptor 2 del factor de crecimiento epidérmico humano negativo (HR+/HER2-), donde el sobretratamiento y el tratamiento insuficiente siguen siendo preocupaciones clínicas.
Los modelos tradicionales suelen depender de factores clinicopatológicos variables y pueden requerir pruebas adicionales o más tiempo. Una herramienta de software de patología digital recientemente autorizada por la FDA proporciona ahora estratificación del riesgo de metástasis a distancia el mismo día para apoyar la planificación terapéutica.
ArteraAI Breast de Artera (Los Altos, CA, EE. UU.) ha recibido la aprobación de la Administración de Alimentos y Medicamentos de EE. UU. (FDA) para su uso en pacientes con cáncer de mama invasivo HR+/HER2- en estadio temprano, y es la primera y única herramienta de estratificación de riesgo basada en patología digital aprobada por la FDA para esta enfermedad. El software genera una puntuación de riesgo derivada de IA que proporciona información pronóstica sobre la probabilidad de metástasis a distancia. Utilizando un umbral de puntuación predefinido, estratifica a las pacientes en grupos de bajo y alto riesgo.
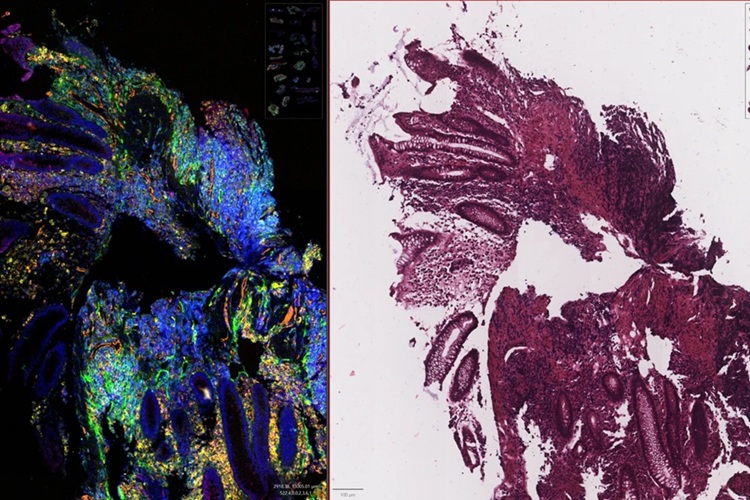
ArteraAI Breast analiza imágenes histopatológicas digitalizadas junto con variables clínicas del paciente para generar la puntuación. Esta herramienta está diseñada para integrarse en los flujos de trabajo patológicos estándar de muestras de resección quirúrgica rutinarias, sin necesidad de tejido adicional ni recolección de muestras por separado. Los resultados se pueden obtener el mismo día, lo que permite a los laboratorios proporcionar información sobre el riesgo pronóstico específico del paciente junto con el informe histopatológico estándar.
La FDA autorizó ArteraAI Breast mediante el procedimiento 510(k), ampliando así la plataforma de la compañía más allá del cáncer de próstata. La autorización de la FDA coincide con la obtención del marcado CE tanto para la prueba de biopsia de próstata ArteraAI como para la prueba de cáncer de mama ArteraAI.
Los datos presentados en el Simposio de Cáncer de Mama de San Antonio de 2025 evaluaron el modelo en cáncer de mama en estadio temprano y destacaron su potencial para ayudar a determinar el beneficio de la quimioterapia en poblaciones de pacientes seleccionadas. Al proporcionar una estratificación de riesgo consistente y basada en la patología en el momento del diagnóstico, el software está diseñado para ayudar a los médicos a contextualizar el riesgo del paciente dentro de los marcos de decisión de tratamiento establecidos.
"La aprobación de la FDA para ArteraAI Breast representa una expansión significativa de nuestra plataforma de IA, ya aprobada por la FDA, en oncología", declaró Andre Esteva, director ejecutivo y cofundador de Artera.
"Este hito refleja el creciente papel de nuestra tecnología en diversos tipos de cáncer. El tratamiento del cáncer de mama es muy complejo, y las decisiones terapéuticas dependen del riesgo individualizado. Nuestro objetivo sigue siendo el mismo para el cáncer de próstata, de mama y otros tipos de cáncer: ayudar a los médicos a traducir datos complejos en decisiones terapéuticas más precisas y personalizadas a lo largo de todo el proceso oncológico".
“Esta autorización representa un avance importante en el camino hacia la personalización de los tratamientos para pacientes con cáncer de mama en etapa temprana”, afirmó el Dr. Eric Winer, oncólogo médico y director del Centro Oncológico de Yale.
“El uso de la IA y la patología digital tiene el potencial de optimizar los flujos de trabajo operativos, a la vez que crea una sólida conexión interdisciplinaria entre oncología y patología. Este enfoque puede mejorar aún más la capacidad de los médicos para ayudar a los pacientes a tomar las mejores decisiones de tratamiento”.
Enlaces relacionados
Artera