Un marcador genético de rutina podría ayudar a guiar la terapia dirigida en la leucemia aguda
Actualizado el 05 May 2026
La leucemia mieloide aguda (LMA) es un cáncer de sangre agresivo con resultados de tratamiento muy variables entre pacientes. Seleccionar a los pacientes que se beneficiarán de los fármacos dirigidos sigue siendo difícil, lo que limita la precisión en la atención rutinaria.
Muchas alteraciones genómicas ya se analizan al momento del diagnóstico, pero pocas indican de forma fiable la respuesta terapéutica. Un nuevo estudio muestra que una mutación evaluada de forma rutinaria puede ayudar a identificar a los pacientes que responden a un fármaco que inhibe la enzima DCPS.
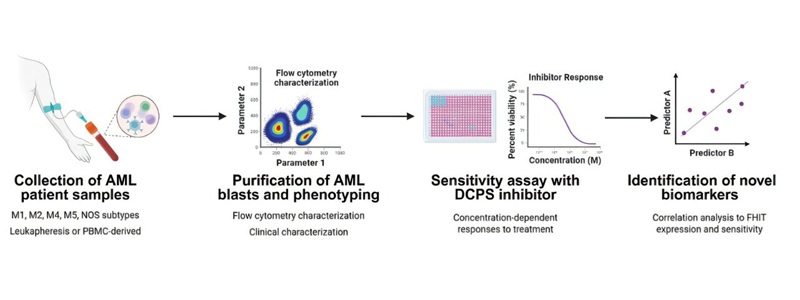
Investigadores del Instituto Karolinska (Estocolmo, Suecia) identificaron niveles bajos de la proteína FHIT como un marcador de sensibilidad a la inhibición de DCPS. Los autores informan que las muestras de pacientes con LMA con niveles reducidos de FHIT responden al tratamiento dirigido a DCPS. También señalan una prueba genética existente —la prueba de mutación IDH2— que puede detectar esta actividad biológica.
La observación clave es que los pacientes con una mutación en IDH2 suelen tener niveles bajos de FHIT y responden mejor a la terapia dirigida a DCPS. Dado que IDH2 ya forma parte de las pruebas diagnósticas de rutina en el diagnóstico de LMA, el marcador puede utilizarse sin necesidad de realizar nuevos análisis. Este enfoque podría simplificar el diseño de los ensayos clínicos al limitar la selección de pacientes a aquellos con mayor probabilidad de beneficiarse.
El equipo analizó 24 muestras primarias de LMA con RG3039, un compuesto que bloquea la actividad de DCPS, y examinó conjuntos de datos de pacientes disponibles públicamente para examinar los vínculos entre la expresión de FHIT y las alteraciones genéticas. En las cohortes de LMA, la proporción con niveles bajos de FHIT osciló entre el 5 % y el 24 %, observándose la mayor proporción en niños.
En el síndrome mielodisplásico (SMD), un trastorno sanguíneo relacionado, aproximadamente el 36 % de los pacientes mostraron silenciamiento del gen FHIT. En conjunto, estos datos sugieren un subgrupo definido en el que la inhibición de DCPS justifica una evaluación específica.
Los hallazgos se publicaron en Discover Oncology. Los investigadores planean validar los resultados en cohortes de pacientes más amplias e investigar más a fondo la conexión biológica entre las mutaciones de IDH2 y la expresión de FHIT. A largo plazo, esperan que estos datos sirvan de base para el diseño de un estudio clínico de terapia dirigida a DCPS en la LMA.
“Muchos fármacos oncológicos prometedores fracasan en ensayos clínicos porque se prueban en grupos de pacientes muy amplios”, afirmó Francesca Grassi, doctoranda del Departamento de Medicina en Huddinge del Karolinska Institutet y primera autora del estudio. “Al utilizar un biomarcador que ya está disponible en la práctica clínica, la selección de pacientes puede hacerse más sencilla y precisa”.
“La mutación IDH2 aporta la información necesaria para identificar a los pacientes adecuados sin necesidad de análisis adicionales. Esto podría facilitar la planificación de futuros ensayos clínicos, especialmente en grupos de pacientes con opciones de tratamiento limitadas”, añadió Grassi.
Enlaces relacionados
Instituto Karolinska