Identifican un “interruptor protector” en el linfoma difuso de células B grandes
Actualizado el 27 Apr 2026
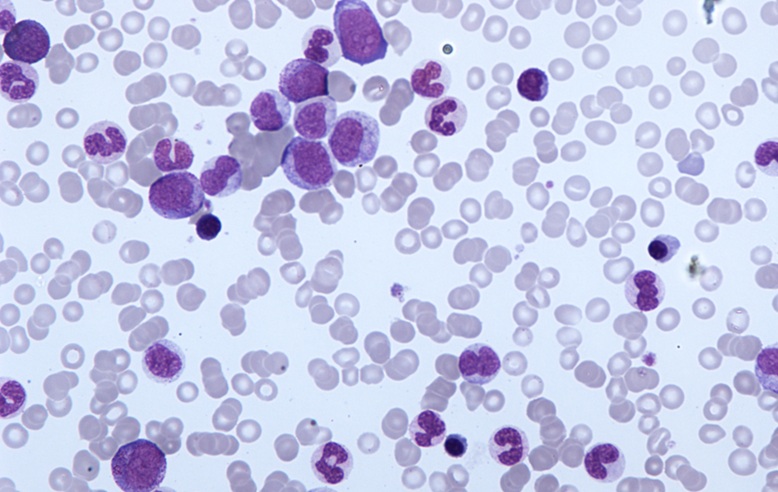
El linfoma difuso de células B grandes (LDCBG) es la forma más común de linfoma no Hodgkin y suele presentar un comportamiento clínico agresivo. Si bien muchos pacientes responden a la quimioterapia estándar (conocida como R-CHOP), los resultados varían y la estratificación del riesgo al momento del diagnóstico sigue siendo un desafío.
Se necesitan nuevos marcadores que reflejen mejor la biología tumoral y orienten las decisiones terapéuticas en la hematopatología de rutina. Un nuevo estudio muestra ahora que la pérdida de una única proteína reguladora puede tanto impulsar la enfermedad como servir como un indicador pronóstico medible.
Investigadores del Instituto de Investigación contra la Leucemia Josep Carreras (IJC; Barcelona, España) han identificado la enzima HDAC7 como un "interruptor de apagado" biológico en el LDCBG, detallando sus hallazgos en The Journal of Immunology. El estudio posiciona la subexpresión de HDAC7 como un posible biomarcador pronóstico e indica que restaurar su expresión suprime el crecimiento maligno en modelos experimentales. Asimismo, subraya el papel esencial de HDAC7 en el desarrollo de un sistema inmunitario saludable.
La investigación explica que la HDAC7 regula la reacción del centro germinal, donde las células B proliferan y maduran para generar respuestas de anticuerpos eficaces. En experimentos con ratones, la eliminación de la HDAC7 de las células B impidió su correcta maduración, dejando a las células estancadas en un estado inmaduro e incapaces de producir los anticuerpos adecuados. Estos resultados respaldan la función de la HDAC7 como regulador principal del desarrollo de las células B en los centros germinales de los ganglios linfáticos.
Los análisis de enfermedades humanas vincularon estos mecanismos con el comportamiento clínico. Al examinar muestras tumorales de pacientes, muchas mostraron niveles reducidos de HDAC7. Los datos de supervivencia de 292 individuos con LDCBG indicaron que la baja expresión tumoral de HDAC7 se asoció con un pronóstico significativamente peor que los tumores con niveles más normales. En conjunto, estas observaciones son consistentes con la hipótesis de que HDAC7 actúa como un freno natural en la progresión de la enfermedad.
Los estudios de restauración funcional confirmaron aún más esta función. Al reintroducir la expresión de HDAC7 en células de LDCBG, la proliferación se detuvo, las células cancerosas sufrieron apoptosis y los tumores se redujeron notablemente al reactivar la proteína. Los autores describen a HDAC7 como un supresor tumoral natural que ayuda a controlar la proliferación de células B.
Los hallazgos describen implicaciones prácticas. La medición de los niveles de HDAC7 en muestras diagnósticas podría servir como biomarcador para predecir la evolución de la enfermedad y personalizar el tratamiento, y la reactivación de HDAC7 se presenta como una estrategia terapéutica potencial.
Los autores señalan que se requieren más estudios confirmatorios. El LDCBG representa aproximadamente el 40 % de los diagnósticos de linfoma no Hodgkin en todo el mundo, y una proporción considerable de pacientes no responde a R-CHOP, lo que subraya la necesidad de mejores herramientas pronósticas y nuevos enfoques terapéuticos.
“Este trabajo identifica a HDAC7 tanto como un elemento clave en el desarrollo normal de las células inmunitarias, como un posible supresor del linfoma. Creemos que puede ayudarnos a clasificar los pacientes con mayor precisión y, a largo plazo, a diseñar nuevas estrategias terapéuticas específicamente dirigidas a quienes más las necesitan”, afirmó la Dra. Maribel Parra, investigadora principal del grupo de desarrollo y enfermedades linfocíticas del IJC.
Enlaces relacionados
Instituto de Investigación contra la Leucemia Josep Carreras