Comparan inmunoanálisis para el diagnóstico de infecciones agudas de tifo murino
Por el equipo editorial de LabMedica en español
Actualizado el 16 Sep 2019
El tifus murino es una enfermedad transmitida por las pulgas y es causada por una bacteria gramnegativa intracelular llamadas Rickettsia typhi; la enfermedad se manifiesta clínicamente con fiebre aguda, escalofríos, dolor muscular, náuseas, vómitos, dolor de estómago, tos y erupción cutánea.Actualizado el 16 Sep 2019
Se necesitan diagnósticos rápidos apropiados para diferenciarla de otras infecciones, ya que el manejo del paciente varía. Debido a la baja rickettsemia durante la enfermedad aguda, la sensibilidad de la reacción en cadena de la polimerasa (PCR) en tiempo real es muy variable. Por lo tanto, el serodiagnóstico mediante el ensayo de inmunofluorescencia (IFA) se mantiene como el estándar de oro.
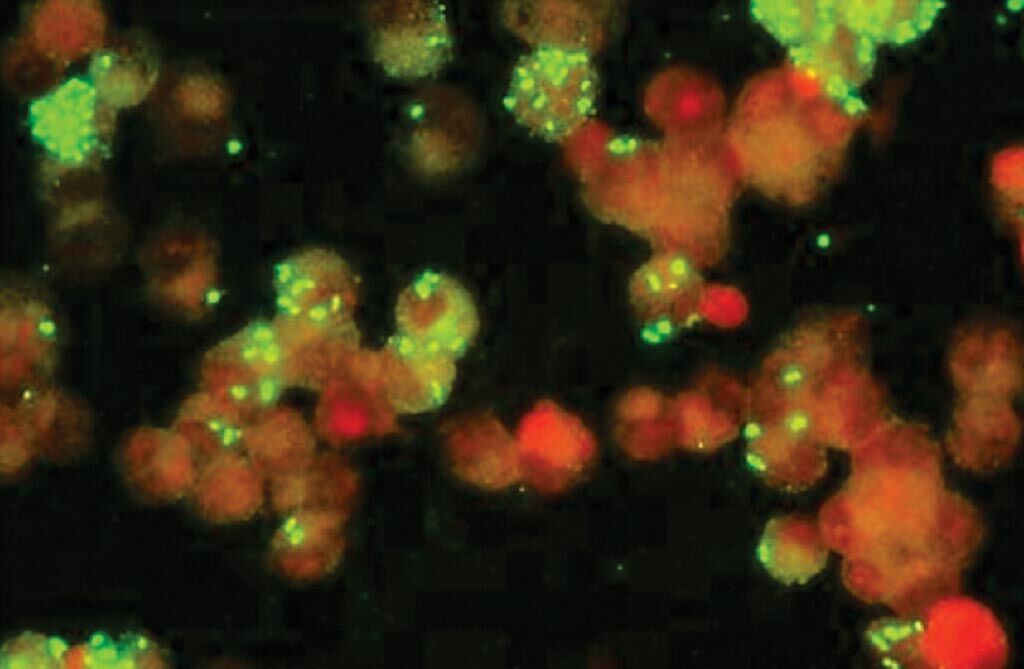
Imagen: Una fotomicrografía de un ensayo de inmunofluorescencia (IFA) para Rickettsia (Fotografía cortesía de Fuller Laboratories).
Los científicos que trabajan con la Asociación de Investigación de Indonesia sobre Enfermedades Infecciosas (Yakarta, Indonesia) obtuvieron muestras de ocho hospitales de enseñanza de referencia del gobierno en siete capitales de provincia. Se usaron muestras de plasma agudas y convalecientes emparejadas de 40 casos confirmados con R. typhi y 58 controles con otro tipo de infección confirmada, para evaluar el desempeño del ensayo inmunoabsorbente ligado a enzimas IgM e IgG (ELISA) y del ensayo IFA. Las 58 muestras de plasma emparejadas usadas para los controles fueron negativas para R. typhi y Rickettsia spp., pero positivas para otros patógenos por cultivo o por pruebas moleculares.
El ensayo de inmunofluorescencia (IFA) se realizó utilizando kits de Focus Diagnostics (Cypress, CA, EUA). La dilución para las muestras de estudio fue 1:64, y para los controles positivos proporcionados fue de 1:32. Las muestras agudas y convalecientes de cada sujeto se realizaron simultáneamente. El plasma agudo y convaleciente se probó simultáneamente usando kits ELISA de Fuller Laboratories (Fullerton, CA, EUA). Los micropozos se recubrieron con la proteína de membrana de la superficie externa rOmp B purificada de R. typhi. La densidad óptica (D.O.) se midió a una longitud de onda de 450 nm (Multiskan GO; ThermoFisher Scientific, Vantaa, Finlandia).
El equipo informó que la sensibilidad y especificidad de la prueba ELISA combinada IgM e IgG anti-R. typhi usando muestras emparejadas fueron excelentes (95,0% y 98,3%, respectivamente), comparables con la prueba de IFA IgM e IgG combinadas (97,5% y 100%, respectivamente); la sensibilidad de la prueba ELISA IgM sola para las muestras agudas fue mala (45,0%), pero la especificidad fue excelente (98,3%). La prueba IFA IgM fue más sensible (77,5%), pero menos específica (89,7%) para las muestras individuales. La IgM se pudo detectar desde el día tres de fiebre usando la prueba ELISA y a partir del día cuatro con la prueba IFA. A partir del día nueve de la enfermedad, la prueba IFA detectó la IgM en todos los casos, mientras que la prueba ELISA pasó por alto dos muestras (días 10 y 25).
Los autores concluyeron que sus datos respaldan la validez de la prueba ELISA en el diagnóstico de infección por R. typhi. Como la especificidad en las muestras agudas, así como la sensibilidad y especificidad en las muestras convalecientes y las muestras emparejadas fueron excelentes, se recomienda la prueba ELISA cuando no es factible realizar las pruebas mediante microscopía de fluorescencia. Sin embargo, la IFA es el método de elección si hay recursos disponibles. La prueba ELISA es apropiada para entornos con recursos limitados, ya que es fácil de leer, es objetiva y tiene un alto rendimiento. El estudio fue publicado el 26 de agosto de 2019 en la revista Vector-Borne and Zoonotic Diseases.
Enlace relacionado:
Asociación de Investigación de Indonesia sobre Enfermedades Infecciosas
Focus Diagnostics
Fuller Laboratories
ThermoFisher Scientific