Secuenciación de próxima generación impacta todos los aspectos de la atención del síndrome mielodisplásico
Por el equipo editorial de LabMedica en español
Actualizado el 24 Nov 2021
El síndrome mielodisplásico (SMD) es un tipo de cáncer de la sangre que afecta la médula ósea. Provoca niveles bajos de uno o más tipos de células sanguíneas en la sangre. El SMD es más común en personas mayores de 70 años, pero puede ocurrir a cualquier edad.Actualizado el 24 Nov 2021
Los signos y síntomas del SMD pueden incluir mareos, fatiga, debilidad, dificultad para respirar, hematomas y sangrado, infecciones frecuentes y dolores de cabeza. El tratamiento de los síndromes mielodisplásicos suele estar destinado a ralentizar la enfermedad, aliviar los síntomas y prevenir complicaciones. Las medidas comunes incluyen transfusiones de sangre y medicamentos para estimular la producción de células sanguíneas.
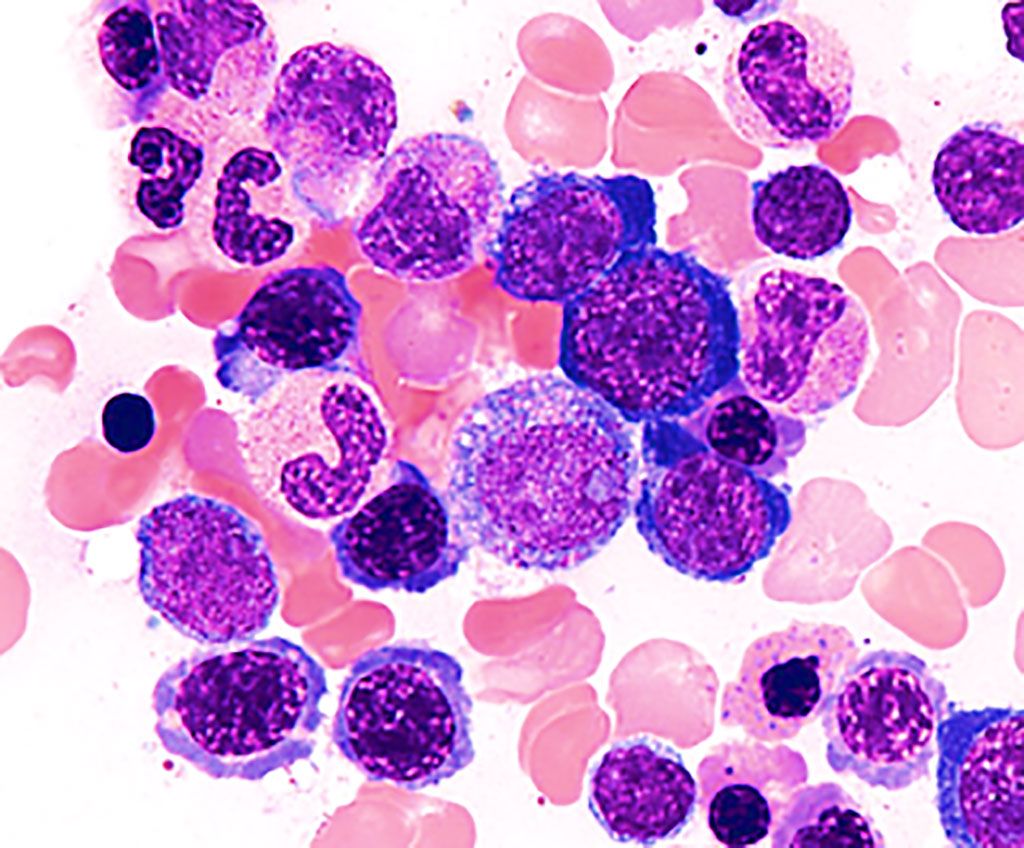
Imagen: Frotis de médula ósea de una persona con síndrome mielodisplásico que muestra una morfología y maduración aberrantes (dismielopoyesis), lo que resulta en una producción ineficaz de células sanguíneas (Fotografía cortesía de Melbourne Blood Specialists)
Los hematólogos del Centro de Cáncer Moffitt (Tampa, FL, EUA) y sus colegas, incorporaron la secuenciación de próxima generación en el estándar de práctica que se requerirá para los pacientes con síndrome mielodisplásico y afectará todas las facetas de la atención. Destacaron las mutaciones de TP53 para mostrar la importancia de la personalización, en particular para los subgrupos que responden mal a la terapia estándar de atención. Identificaron el estado de mutación de TP53 y la frecuencia de alelos variantes como predictores de supervivencia entre pacientes con síndrome mielodisplásico y leucemia mieloide aguda secundaria. El grupo de riesgo muy adverso, que representa la mayoría de los pacientes, está formado por aquellos con una alta frecuencia de alelos variantes del 40%, cariotipo complejo o más de una mutación o una mutación en el contexto de TP53.
Los científicos señalaron que los médicos pueden esperar los resultados de los paneles de secuenciación para la gran mayoría de los pacientes con síndrome mielodisplásico, y agregaron que el tiempo de respuesta cada vez es mejor. Mientras tanto, otros factores que pueden proporcionar una alta probabilidad previa a la prueba de si un paciente puede tener una mutación en TP53 incluyen antecedentes relacionados con la terapia, anomalías múltiples, anemia refractaria, exceso de blastos con aumento de sideroblastos anillados e inmunohistoquímica de p53. Otras mutaciones que potencialmente podrían ser dirigidas incluyen mutaciones en IDH1 e IDH2, que son raras en el síndrome mielodisplásico, y mutaciones de empalme.
Para mejorar los resultados de este subconjunto molecular de pacientes, los científicos investigan eprenetapopt, el primer reactivador de p53 de su clase. Los resultados de un estudio de fase 2 mostraron que el agente en combinación con la azacitidina indujo respuestas en más del 70% de los pacientes, con tasas de remisión completa del 40% al 50%. Sin embargo, el estudio de fase 3 no cumplió con su criterio de valoración principal de mejora de la remisión completa, como otros ensayos de combinaciones novedosas, que incluyen el agente, están en curso y los investigadores mantienen la esperanza.
David A. Sallman, MD, hematólogo y autor principal del estudio, dijo: “Realmente pensamos que, en el futuro, particularmente en el contexto de una terapia novedosa, el logro de la depuración de p53, lo más bajo posible, potencialmente en ese punto y luego en un puente al trasplante, puede ser el método definitivo”. El estudio se presentó en el 39º Simposio Anual de la Fundación de Quimioterapia que se celebró del 3 al 5 de noviembre de 2021, en Nueva York, NY, EUA.
Enlace relacionado:
Centro de Cáncer Moffitt