Mapean el paisaje inmunogenómico de las neoplasias hematológicas
Por el equipo editorial de LabMedica en español
Actualizado el 20 Jul 2020
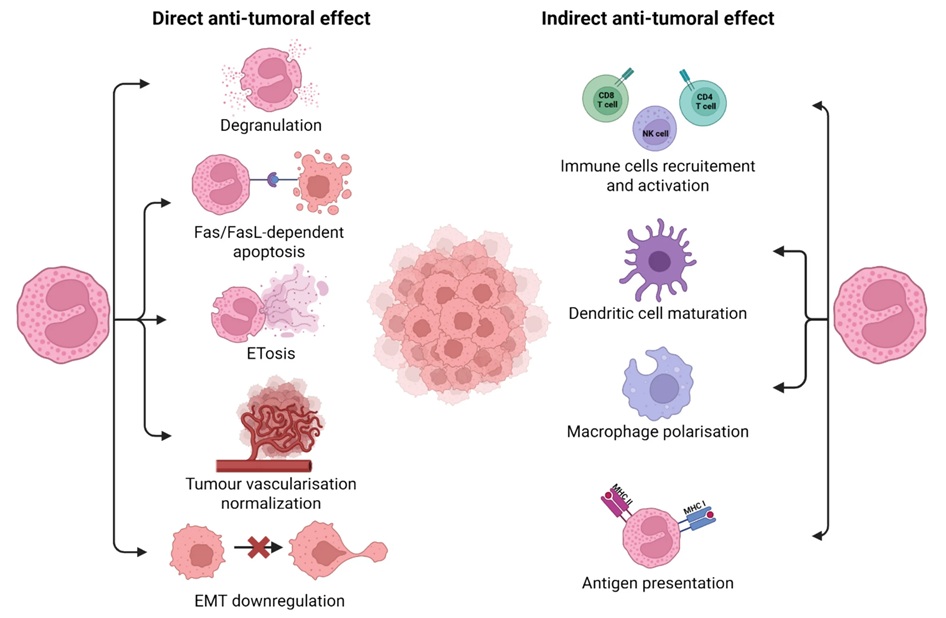
Se puede considerar la reacción del sistema inmune del cuerpo contra el cáncer como un ciclo. Las células cancerosas contienen proteínas que difieren de las proteínas en otros tejidos. Sus componentes, conocidos como antígenos, deben ser presentados a las células T del sistema inmune por las células cancerosas.Actualizado el 20 Jul 2020
Cuando identifican antígenos, las células T se activan y comienzan a destruir las células cancerosas, lo que hace que estas liberen más antígenos, mejorando aún más la respuesta inmune. Además de las células T, las células natural killer (NK) tienen la capacidad de destruir las células. En inmunoterapias, el sistema inmune se activa terapéuticamente estimulando diferentes etapas del ciclo.
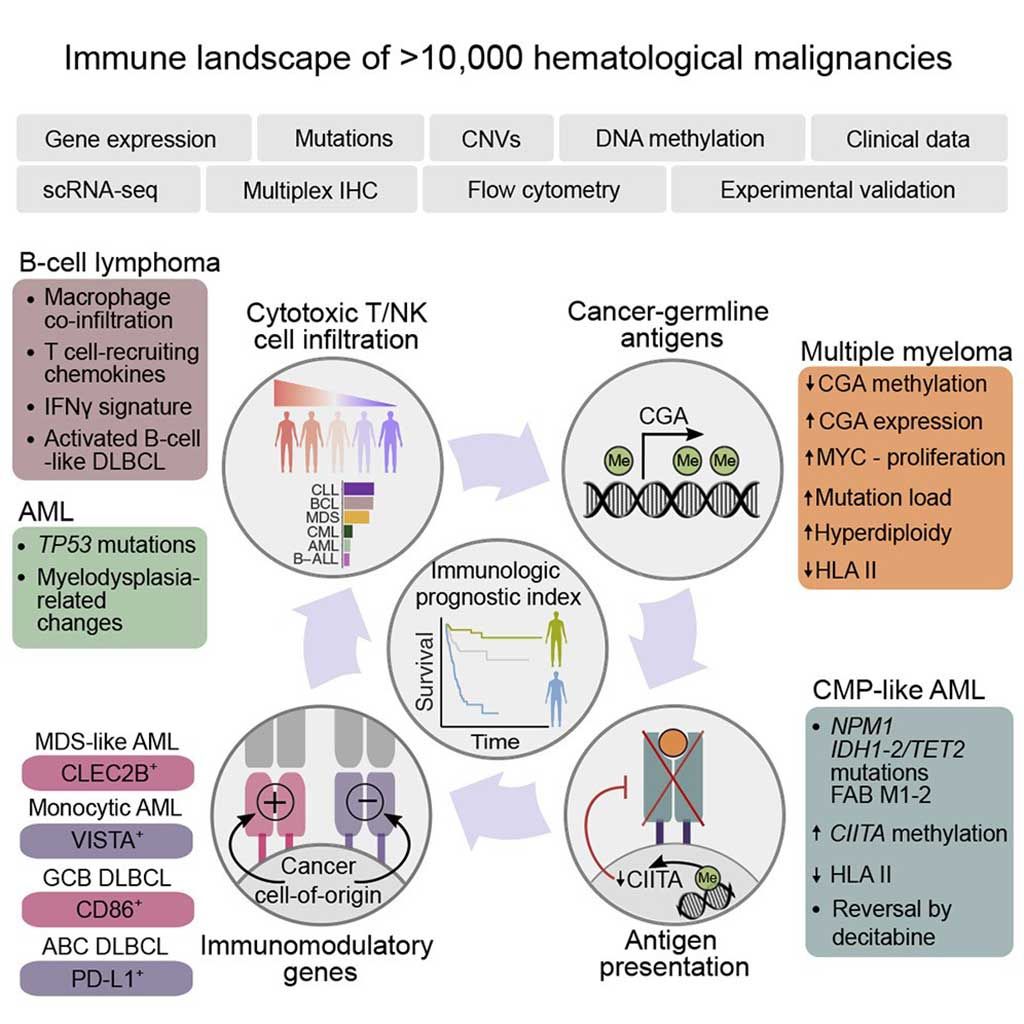
Imagen: El paisaje inmunogenómico de las neoplasias hematológicas (Fotografía cortesía del Hospital Universitario de Helsinki).
Un gran equipo de científicos médicos que colaboran con el Hospital Universitario de Helsinki (Helsinki, Finlandia), integró más de 8.000 transcriptomas y 2.000 muestras con genómica de varios niveles de cánceres hematológicos, para investigar cómo las características inmunológicas están relacionadas con los subtipos de cáncer, las alteraciones genéticas y epigenéticas y la supervivencia de los pacientes y validaron hallazgos clave. Mapearon el paisaje inmune de las neoplasias hematológicas en un conjunto de datos que abarca más de 10.000 pacientes para identificar objetivos farmacológicos y grupos de pacientes que se podrían beneficiar con las inmunoterapias.
El equipo informó que la infiltración de linfocitos citotóxicos se asoció con TP53 y los cambios relacionados con la mielodisplasia en la leucemia mieloide aguda, y el fenotipo tipo células B activadas y la respuesta del interferón-γ en el linfoma. La presentación del antígeno regulada por la metilación de CIITA, los puntos de control inmunes específicos del tipo de cáncer, como el supresor Ig del dominio V de la activación de células T (VISTA) en neoplasias mieloides y la variación en la expresión del antígeno del cáncer contribuyeron aún más a la heterogeneidad inmune y a la supervivencia prevista.
Los investigadores encontraron que, en ciertos subtipos de leucemia mieloide aguda, la metilación del ADN tenía una presentación de antígeno epigenéticamente silenciada. Un medicamento que inhibe la metilación del ADN restableció la expresión de proteínas presentadoras de antígeno en pruebas de laboratorio. Como el medicamento ya se usa para tratar la leucemia mieloide aguda, podría aumentar potencialmente la eficacia de las inmunoterapias mediante el uso combinado.
Satu Mustjoki, MD, PhD, profesor de hematología traslacional y autor principal del estudio, dijo: “La extensa encuesta de las características inmunogenómicas de las neoplasias hematológicas realizadas en el estudio ayuda a los científicos y médicos a enfocar las inmunoterapias en los grupos de pacientes que obtienen el mayor beneficio y además comprender los factores que tienen un impacto potencial sobre la eficacia de las terapias”.
Los autores concluyeron que su estudio proporcionó un recurso que vincula la inmunología con los subtipos de cáncer y la genómica en las neoplasias hematológicas. El estudio fue publicado el 9 de julio de 2020 en la revista Cancer Cell.
Enlace relacionado:
Hospital Universitario de Helsinki