Riesgo de desarrollar inhibidores contra el factor VIII es afectado por la genética
Por el equipo editorial de LabMedica en español
Actualizado el 11 Sep 2019
Para los pacientes con hemofilia A (HA) severa, el estándar de atención actual incluye infusiones profilácticas regulares de productos de factor VIII (FVIII) para prevenir hemorragias espontáneas o infusiones a demanda para tratar hemorragias.Actualizado el 11 Sep 2019
Muchos factores, como los relacionados con los pacientes, la enfermedad o el producto, podrían influir sobre el riesgo potencial de inmunogenicidad de los bioterapéuticos, pero las contribuciones relativas de estos factores al desarrollo de anticuerpos neutralizantes actualmente no se comprenden completamente. Varios factores de riesgo de inhibición contra los productos de FVIII están bien reconocidos, como el tipo de mutación del gen del factor VIII (F8).
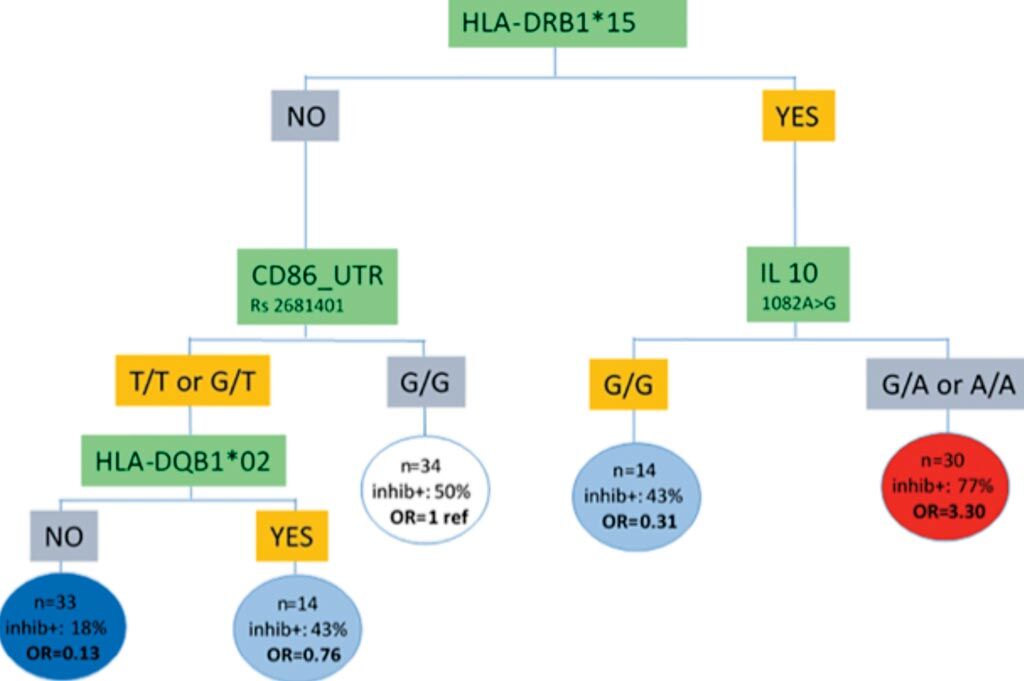
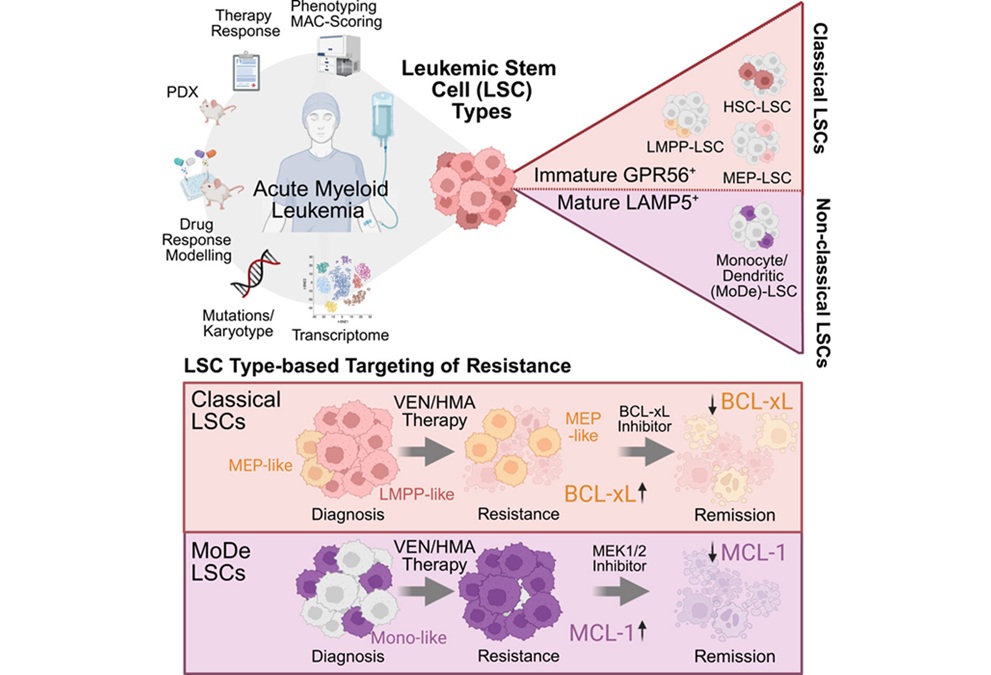
Imagen: Estratificación de riesgo integrando datos genéticos para el desarrollo de inhibidores del factor VIII en pacientes con hemofilia severa (Fotografía cortesía de la Universidad Paris-Saclay).
Un grupo internacional de científicos dirigido por la Universidad Paris-Saclay (Villejuif, Francia), analizó datos de pacientes con hemofilia A severa de dos centros alemanes en Bonn y Frankfurt, que fueron reclutados para la base de datos europea, ABIRISK tranSMART. Los científicos investigaron los componentes clínicos y genéticos detrás del desarrollo de inhibidores contra el factor VIII, buscando específicamente aquellos genes que estuvieran relacionados con el sistema inmune. En total, 593 pacientes con HA grave de la base de datos de Bonn y 79 de la base de datos de Frankfurt fueron incluidos en el presente estudio.
La tipificación de los antígenos HLA clase II (HLA-DRB1, HLA-DQB1) se realizó mediante la metodología de reacción en cadena de la polimerasa (PCR) con cebador específico de secuencia (SSP) (Olerup SSP AB, Estocolmo, Suecia). Las variantes de polimorfismo de nucleótido único (SNP) para IL-10 1082A> G (rs1800896), CTLA4 CT60A>G (rs3087243), TNF 308G>A (rs1800629), CD32 500 A>G (rs1801274), MAPK9 (rs4147385) fueron genotipificadas. Para el gen CD86, se investigaron cuatro SNP bialélicos: rs2715267 en la región promotora, rs2681417 en la región del exón 4, rs1129055 en la región del exón 7 y rs2681401 en la región transcrita no traducida (UTR).
En total, se analizaron 586 pacientes de Bonn, de los que 113 (19%) desarrollaron inhibidores, y 79 de Frankfurt, de los que 32 pacientes (41%) desarrollaron inhibidores. El análisis reveló que los pacientes de Bonn que tenían antecedentes familiares de desarrollo de inhibidores tenían un riesgo 5,94 veces mayor de desarrollar inhibidores, en comparación con los pacientes sin antecedentes familiares de una respuesta inmune contra el factor VIII. La historia familiar no estaba disponible para los pacientes de Frankfurt. Aunque no es significativo en los datos de los dos centros, el equipo observó que los pacientes con un tipo de sangre distinto de O tenían 1,46 más probabilidades de desarrollar inhibidores.
En un análisis de 142 pacientes de la base de datos de Bonn, mostraron que los pacientes con un haplotipo HLA específico (llamado HLA-DRB1*15), y con un SNP particular en el gen IL-10, tenían un mayor riesgo de desarrollar inhibidores. De 30 pacientes en este grupo, 23 desarrollaron una respuesta inmune contra el factor VIII. Los pacientes negativos para los haplotipos HLA-DRB1*15 y HLA-DQB1*02, y para ciertos SNP en el gen, tenían el riesgo más bajo, con solo cuatro de 36 pacientes dentro de este subgrupo que desarrollaron inhibidores.
Los autores concluyeron que el modelo final óptimo, híbrido, basado en el árbol, permite diferenciar a dos grupos de pacientes: un grupo de alto riesgo de inmunogenicidad con HLA-DRB1*15 positivo e IL-10 genotipo G/A y A/A, un grupo de bajo riesgo para la inmunogenicidad con HLADRB1*15 / HLADQB1*02 negativo y CD86 genotipo T/T y G/T. El estudio fue publicado originalmente el 13 de junio de 2019 en la revista PLOS ONE.
Enlace relacionado:
Universidad Paris-Saclay
Olerup SSP AB