Asocian niveles enzimáticos con supervivencia en mieloma múltiple
Por el equipo editorial de LabMedica en español
Actualizado el 08 Feb 2018
El mieloma múltiple (MM) es el segundo cáncer de sangre más común en los EUA, entre el 30% y el 50% de los pacientes con mieloma múltiple tienen copias adicionales del gen que codifica la enzima Adenosina Deaminasa ARN específica (ADAR1).Actualizado el 08 Feb 2018
La enzima ADAR1 se expresa normalmente durante el desarrollo fetal para ayudar a las células sanguíneas a formarse. ADAR1 edita la secuencia de ARN, un tipo de material genético relacionado con el ADN. Al intercambiar un bloque de creación de ARN por otro, ADAR1 altera las células del sistema cuidadosamente orquestadas para controlar qué genes se activan o desactivan y el momento en que lo hacen.
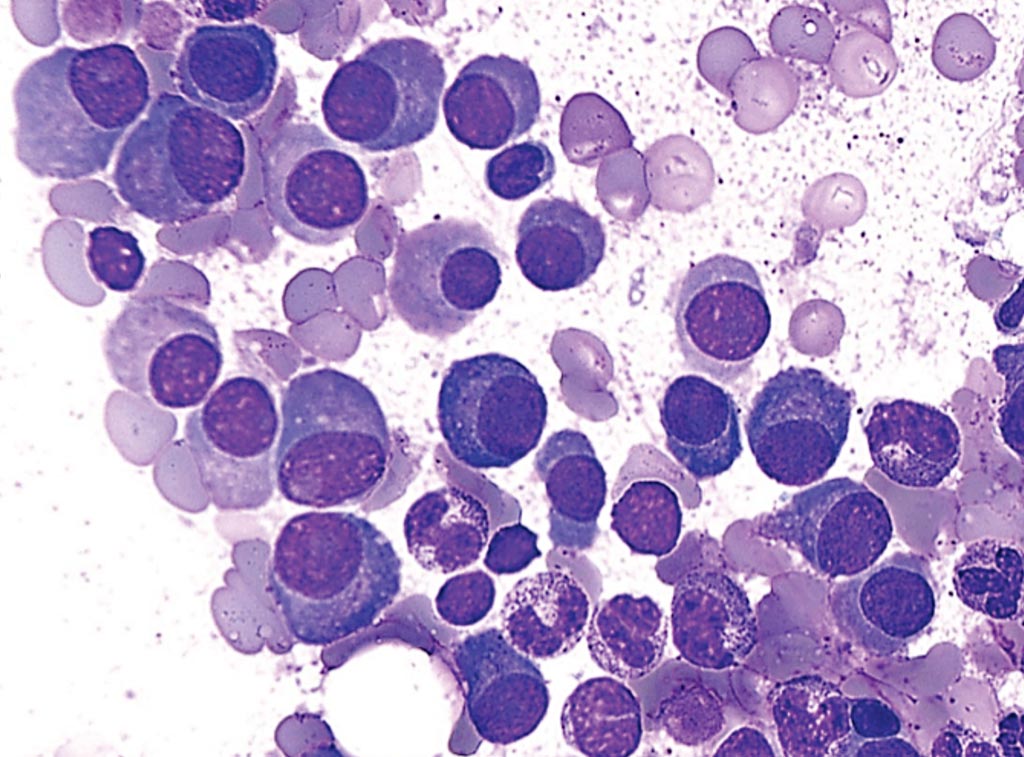
Imagen: Biopsia de médula ósea de un paciente con mieloma múltiple, que muestra infiltración difusa por células plasmáticas neoplásicas, que puede ser reconocida por el núcleo excéntrico y el halo perinuclear (Fotografía cortesía del Dr. Michael G. Bayerl).
Científicos de la Facultad de Medicina de la Universidad de California en San Diego (La Jolla, CA, EUA) obtuvieron muestras de médula ósea de pacientes con MM y controles normales emparejados por edad. Las muestras de sangre periférica (SM) o médula ósea (MO) fueron procesadas mediante centrifugación de densidad de Ficoll y se recogieron células mononucleares totales viables (MNC) para análisis adicionales que se almacenaron en nitrógeno líquido. El diseño del cebador del ensayo de reacción en cadena de polimerasa en tiempo real cuantitativa en tiempo real (RESSq-PCR) tuvo en cuenta los loci específicos del cáncer y los asociados a las células madre. El equipo realizó varios otros procedimientos moleculares para confirmar sus resultados.
Los científicos analizaron una base de datos de casi 800 muestras de pacientes con mieloma múltiple y descubrieron que 162 pacientes con niveles bajos de ADAR1 en sus células tumorales sobrevivieron significativamente más durante un período de tres años en comparación con 159 pacientes con niveles altos de ADAR1. Mientras que más del 90% de los pacientes con niveles bajos de ADAR1 sobrevivieron más de dos años después de su diagnóstico inicial, menos del 70% de los pacientes con niveles altos de ADAR1 estaban vivos después del mismo período de tiempo.
El equipo encontró que dos eventos convergen para activar ADAR1 en el mieloma múltiple, una anomalía genética y señales inflamatorias del tejido de la médula ósea circundante. Juntas, estas señales activan ADAR1, que edita ARN específico de una manera que estabiliza un gen que puede hacer que las células madre del cáncer sean más agresivas. También encontraron que silenciar el gen ADAR1 en el modelo de xenoinjerto redujo la regeneración del mieloma múltiple. Se autorenovaron cinco a diez veces menos células tumorales en ratones que carecían de ADARI, lo que sugiere un nuevo objetivo terapéutico.
Catriona HM Jamieson, MD, PhD, profesora de medicina y autora principal del estudio, dijo: “En los últimos años se han hecho varios avances importantes que son buenas noticias para los pacientes con mieloma múltiple, pero esos nuevos fármacos solo se dirigen a las células cancerosas diferenciadas terminalmente y por lo tanto solo pueden reducir la mayor parte del tumor; no llegan a la causa raíz del desarrollo de la enfermedad, de la progresión y de la recaída: las células madre del cáncer, en la forma en que inhibir ADAR1 lo hace. Me gusta llamar a nuestro método ‘medicina regenerativa de precisión’”. El estudio fue publicado el 4 de diciembre de 2017 en la revista Nature Communications.