Prueba confirma presencia de anticuerpos contra virus linfotrópico de células-T humanas I/II
Por el equipo editorial de LabMedica en español
Actualizado el 26 Jan 2015
Se ha licenciado una prueba suplementaria para el virus linfotrópico de células-T humanas I/II, para ser usada como una prueba adicional, más específica, en muestras de suero o plasma, humanos, que han dado previamente resultados positivos en otras pruebas de diagnóstico primario en bancos de sangre para anticuerpos anti-HTLV-I/II.Actualizado el 26 Jan 2015
Los virus linfotrópicos de células T humanas (HTLV) son un grupo de los retrovirus humanos conocidos por causar enfermedades tales como la leucemia de células T del adulto/linfoma, que es una forma rara de cáncer de la sangre y la inflamación de los nervios en la médula espinal, conocida como mielopatía, así como otras condiciones tales como uveítis y dermatitis infecciosa.
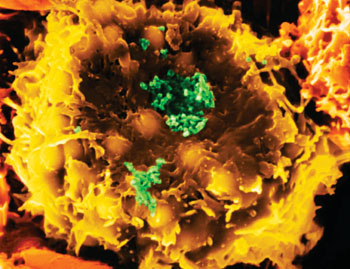
Imagen: Microfotografía electrónica de barrido (SEM) del virus linfotrópico de célula-T humanas-1(HTLV-1) (verde), infectando un linfocito-T (amarillo) (Fotografía cortesía del Dr. Dennis Kunkel).
El HTLV puede transmitirse de persona a persona a través de la lactancia materna, el contacto sexual sin protección, o la transfusión de sangre de un donante infectado. La Dirección de Alimentos y Medicamentos de los EUA(FDA, Silver Springs, MD, EUA), que ha aprobado la prueba, requiere que a la sangre donada le hagan la prueba de anticuerpos para el HTLV-I/II. Actualmente hay dos pruebas de detección con licencia por la FDA para el HTLV-I/II. Si la prueba es positiva, la donación se descarta y se notifica al donante de su rechazo.
La prueba MP Diagnostics HTLV Blot 2.4 (MP Biomedicals Asia Pacific Pte Ltd.; Singapur), es una prueba de inmunoensayo enzimático cualitativo, que les ofrece a los centros de transfusión sanguínea información adicional para transmitir al donante; específicamente, la prueba puede confirmar la infección por HTLV y determinar cuál es el tipo de virus que está causando la infección: HTLV-I o HTLV-II. Muchas personas que están infectadas con HTLV no son conscientes de la infección debido a que el virus puede no causar síntomas o signos de infección. Además, muchas personas infectadas con HTLV-I o HTLV-II pueden no desarrollar nunca alguna enfermedad causada por los virus. Sin embargo, estos portadores asintomáticos pueden transmitir el virus a otras personas.
Karen Midthun, MD, directora del Centro para la Evaluación e Investigación Biológica de la FDA, dijo: “La aprobación de la prueba MP Diagnostics HTLV Blot 2.4 ayudará a los centros de transfusión a aconsejar mejor a los donantes que han tenido resultados positivos en una prueba de detección licenciada por la FDA, para el HTLV-I/II”.
Enlace relacionados:
US Food and Drug Administration
MP Biomedicals Asia Pacific Pte Ltd.