Simple análisis de sangre diagnostica cáncer de pulmón 10 veces más rápido
Actualizado el 10 Oct 2024
Los exosomas (pequeñas vesículas liberadas por las células que contienen proteínas, ADN o fragmentos de ARN) que antes se consideraban desechos celulares se han convertido en actores vitales en la comunicación entre células durante la última década. Mientras que los exosomas de las células sanas transmiten señales importantes por todo el cuerpo, los de las células cancerosas pueden facilitar la propagación de los tumores al preparar los tejidos para recibir las células tumorales antes de que lleguen. Los exosomas transportan proteínas tanto en su interior como en su superficie, y estas proteínas de superficie suelen ser quirales, lo que significa que tienen una torsión hacia la derecha o hacia la izquierda, lo que influye en la forma en que interactúan con la luz. En los exosomas cancerosos, estas proteínas de superficie suelen estar mutadas, lo que significa que la estructura molecular de la proteína ha sido alterada por cambios genéticos. Estas mutaciones afectan sutilmente la forma de la proteína, lo que a su vez cambia su quiralidad. Estas alteraciones se pueden detectar analizando cómo interactúan las proteínas con la luz polarizada circularmente, que puede "coincidir" con la torsión de las proteínas. Cuando la torsión se alinea, se devuelve una señal intensa a un detector de luz. Sin embargo, estas señales de luz suelen ser débiles y difíciles de interpretar, y detectar los exosomas implica extraerlos de muestras de sangre, lo que supone un reto debido a su diminuto tamaño, que oscila entre apenas 30 y 200 nanómetros.
Investigadores de la Universidad de Michigan (Ann Arbor, MI, EUA) han desarrollado un microchip capaz de capturar exosomas del plasma sanguíneo para detectar el cáncer de pulmón. Este nuevo método de diagnóstico, que utiliza una simple extracción de sangre, es diez veces más rápido y catorce veces más sensible que los métodos anteriores, según el equipo de investigación. Para identificar los exosomas, el equipo diseñó nanopartículas de oro en forma de discos retorcidos, adaptadas para capturar exosomas dentro de una cavidad central. Estas cavidades están diseñadas para coincidir perfectamente con el tamaño, la forma y la química de la superficie de los exosomas, lo que permite una captura confiable. Con un giro hacia la derecha, las nanopartículas resuenan fuertemente con la luz que gira hacia la derecha, pero reflejan poca señal cuando se exponen a la luz que gira hacia la izquierda, un fenómeno conocido como dicroísmo circular. Una vez que los exosomas quedan atrapados en las cavidades, las proteínas que transportan pueden amplificar o disminuir la señal de retorno en función de su forma.
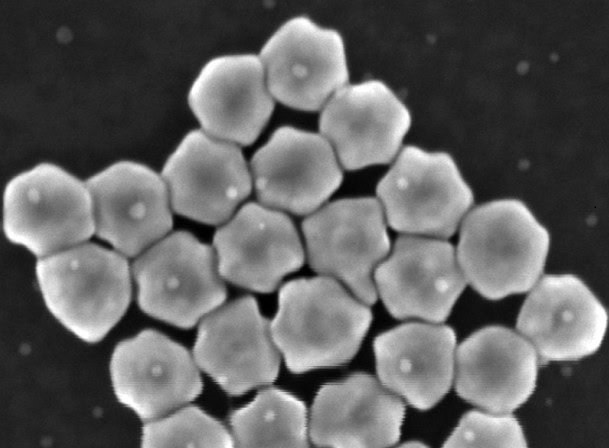
Las cavidades de nanopartículas de oro, dispuestas a lo largo de los diminutos canales de un chip microfluídico, capturaron con éxito exosomas del plasma sanguíneo y diferenciaron entre muestras de individuos sanos y de aquellos con cáncer de pulmón, como se informó en la revista Matter. Los chips microfluídicos, llamados chips CDEXO (detección de EXOsomas mediante dicroísmo circular), también podrían distinguir mutaciones específicas del cáncer de pulmón, lo que ayudaría a los médicos a adaptar los tratamientos para atacar las mutaciones más prevalentes a medida que evolucionan. Los investigadores prevén que el chip CDEXO se utilice inicialmente junto con los métodos de diagnóstico tradicionales, con el potencial de ampliar su uso para detectar otros cánceres, mejorando los esfuerzos de detección temprana a medida que aumenta la confianza en la tecnología.
"Como próximo paso, queremos observar la mayoría de las proteínas mutadas de tumores sólidos conocidas para entender en qué se diferencian sus firmas espectrales", dijo Sunitha Nagrath, profesora de ingeniería química y biomédica de la UM y coautora del estudio. "A partir de aquí, podemos impulsar la tecnología para aumentar aún más esas diferencias espectrales y distinguir entre proteínas".