Grupos de metilación del ADN del meningioma identifican causantes biológicos y vulnerabilidades terapéuticas
Actualizado el 26 May 2022
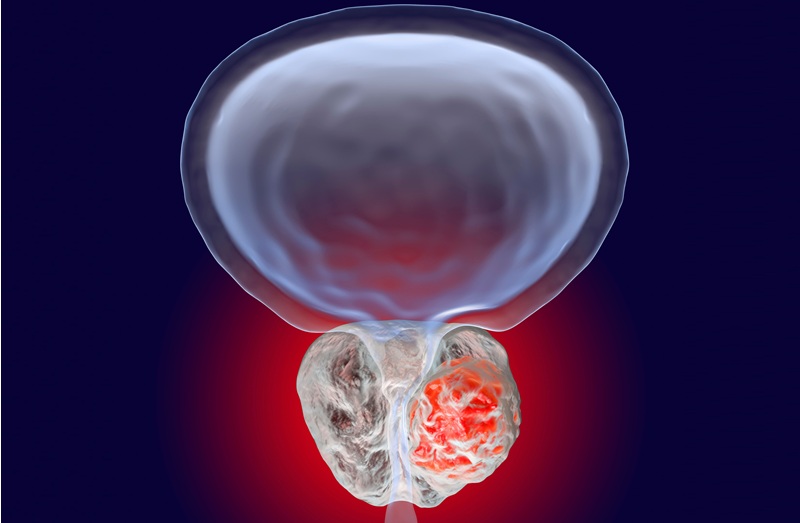
El meningioma, también conocido como tumor meníngeo, suele ser un tumor de crecimiento lento que se forma a partir de las meninges, las capas membranosas que rodean el cerebro y la médula espinal. Los síntomas dependen de la ubicación y ocurren como resultado de la presión del tumor sobre el tejido cercano.
Muchas personas tienen meningiomas, pero permanecen asintomáticos, por lo que los meningiomas se descubren durante una autopsia. Entre uno y dos por ciento de todas las autopsias revelan meningiomas que los individuos desconocían durante su vida, ya que nunca hubo síntomas.
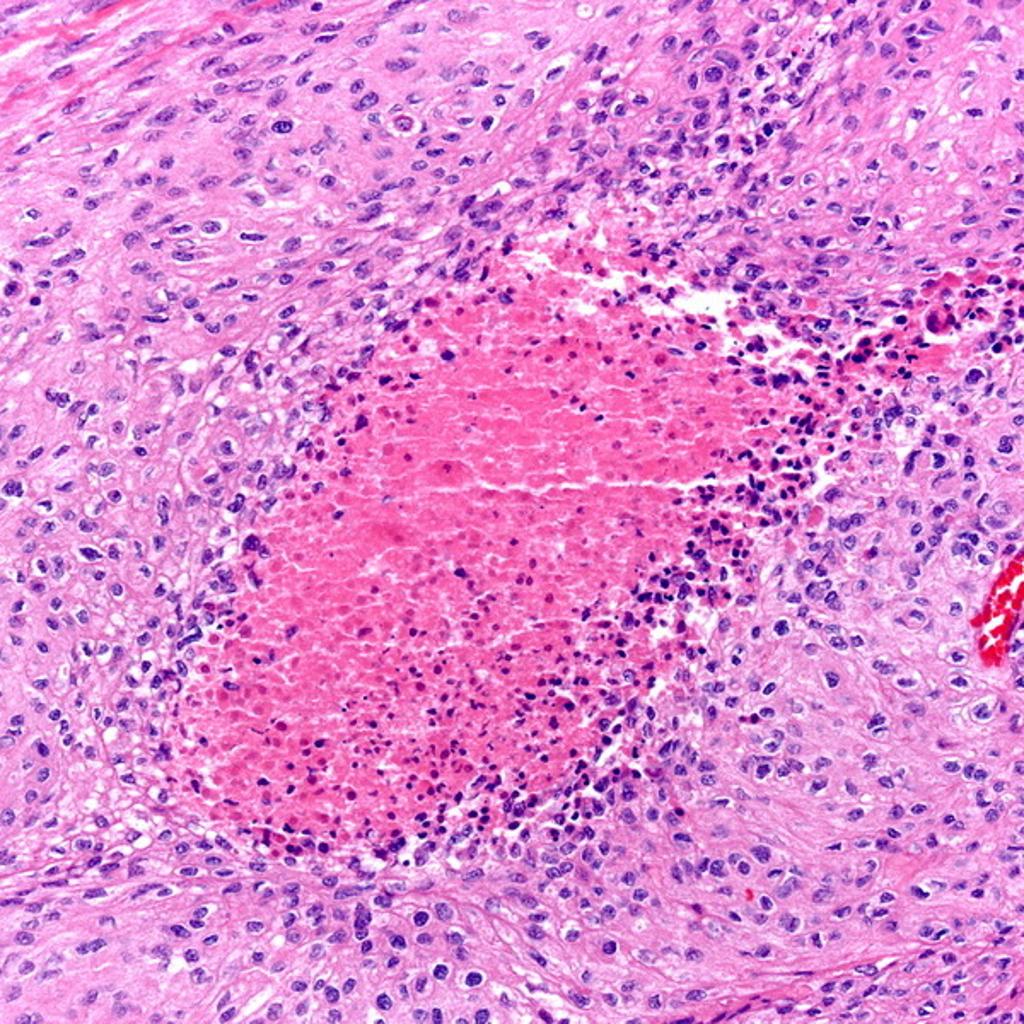
Un gran equipo de científicos médicos dirigido por los de la Universidad de California en San Francisco (San Francisco, CA, EUA) identificó tres grupos de meningiomas basados en la metilación del ADN con un estudio de perfil epigenético que tomó en cuenta otras características moleculares, incluidos los perfiles de variantes del número de copias (CNV) de los tumores intracraneales primarios.
El equipo realizó un perfil de metilación basado en matriz en muestras de 565 pacientes con meningioma tratados en dos centros en los EUA y Hong Kong entre principios de la década de 1990 y 2019. El equipo utilizó un proceso llamado SeSAMe para tener en cuenta los efectos de la CNV en la metilación antes de analizar los datos de metilación junto con secuenciación dirigida, secuenciación del exoma, secuenciación de inmunoprecipitación de cromatina, perfiles transcriptómicos y proteómicos, y otros datos sobre un subconjunto de tumores de meningioma.
Los análisis moleculares integrados del equipo destacaron el meningioma intacto de Merlin, el meningioma inmunoenriquecido y los grupos de meningioma hipermitótico. Junto con las comparaciones con los grupos de metilación definidos por análisis que no tuvieron en cuenta las CNV, el grupo investigó más a fondo con la edición de genes basada en CRISPR y otros estudios funcionales. En contraste con los meningiomas que surgen en pacientes con neurofibromatosis tipo 2 a los que les falta un gen NF2 que codifica para la proteína supresora de tumores Merlin, los científicos encontraron que más de un tercio de los meningiomas caían en un grupo de intacto de Merlin con los resultados clínicos más favorables y vulnerabilidad a la terapia citotóxica.
Los investigadores clasificaron el 28 % de los tumores en un grupo de meningioma hipermitótico relacionado con la resistencia a la terapia citotóxica y malos resultados. Los tumores restantes, casi el 40 % del conjunto de meningiomas, cayeron en un grupo inmunoenriquecido marcado por infiltración de células inmunitarias, características de los vasos linfáticos y resultados de supervivencia intermedios. Con una serie de análisis de seguimiento, vieron signos de que los tumores clasificados en grupos de resultados deficientes o intermedios pueden ser particularmente aptos para responder a los tratamientos con inhibidores del ciclo celular.
David Raleigh, MD, PhD, profesor asistente y autor principal del estudio, dijo: "Estos hallazgos subrayan la importancia del perfil de metilación del ADN para los pacientes con meningioma, lo que finalmente permite la selección o inscripción de ensayos clínicos de inhibidores del ciclo celular u otras terapias moleculares”. El estudio fue publicado el 9 de mayo de 2022 en la revista Nature Genetics.
Enlaces relacionados:
Universidad de California en San Francisco