Mutaciones en las células sanguíneas son responsables de una enfermedad autoinflamatoria severa
Por el equipo editorial de LabMedica en español
Actualizado el 11 Nov 2020
Los trastornos autoinflamatorios graves de inicio en la edad adulta a menudo se manifiestan con características clínicas superpuestas. Las personas afectadas pueden desarrollar episodios de fiebre alta y en picos, una erupción de color rosa o salmón, dolor en las articulaciones, dolor muscular, dolor de garganta y otros síntomas asociados con la enfermedad inflamatoria sistémica.Actualizado el 11 Nov 2020
El diagnóstico de la enfermedad autoinflamatoria grave de aparición en el adulto es difícil porque no existen pruebas específicas o hallazgos de laboratorio (histopatológicos) que permiten diferenciar claramente el trastorno de otros similares. Las personas afectadas suelen tener niveles elevados de glóbulos blancos y/o plaquetas o niveles bajos de glóbulos rojos.
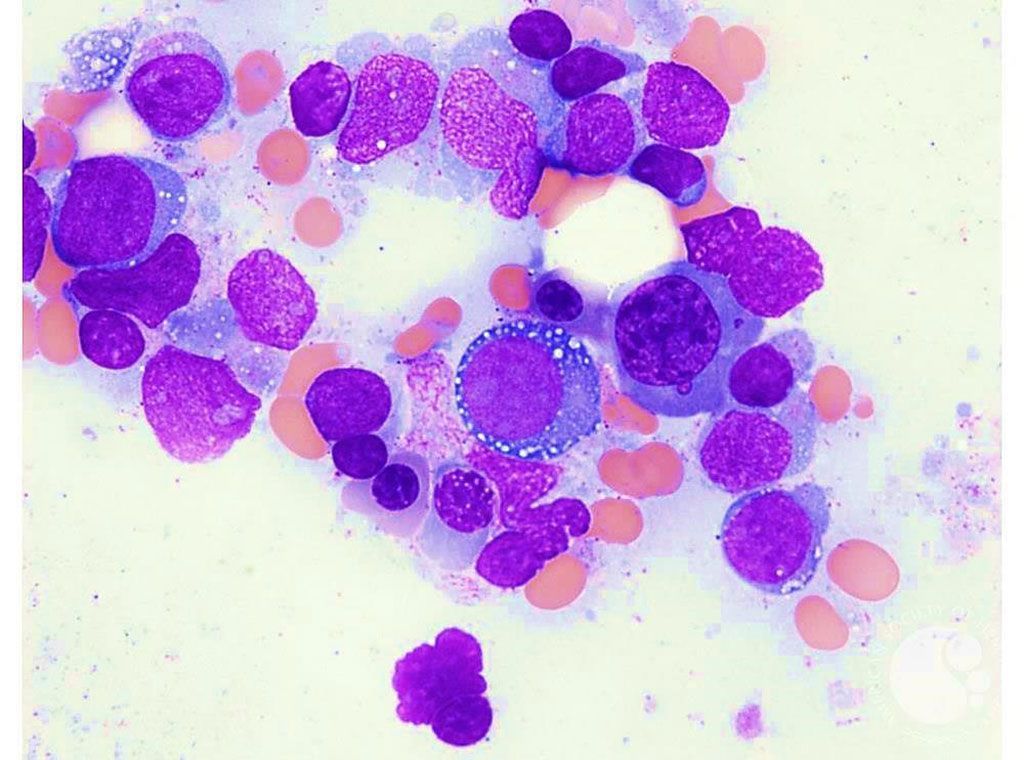
Imagen: Los precursores eritroides vacuolados en la médula ósea a veces se encuentran en pacientes con un trastorno autoinflamatorio grave de inicio en la edad adulta (Fotografía cortesía de Teresa S. Scordino, MD).
Los científicos del Instituto Nacional de Investigación del Genoma Humano (Bethesda, MD, EUA) y sus colegas, analizaron los datos de la secuencia del exoma de sangre periférica, independientemente del fenotipo clínico y el patrón de herencia para identificar mutaciones deletéreas en genes relacionados con la ubiquitina. Realizaron secuenciación de Sanger, inmunotransferencia, pruebas inmunohistoquímicas, citometría de flujo y perfiles de transcriptomas y citoquinas. Los datos de los pacientes consistieron en exomas y genomas de casi 1.500 personas con trastornos autoinflamatorios no diagnosticados y de aproximadamente 1.100 pacientes con trastornos atípicos.
En tres pacientes varones, el equipo descubrió variantes novedosas en el gen UBA1, que reside en el cromosoma X y codifica la enzima E1 que inicia la ubiquitilación de proteínas. Sorprendentemente, el mismo codón, metionina-41, se vio afectado en los tres casos. Además, los tres pacientes tenían vacuolas inusuales en sus células precursoras eritroides y mieloides, que no se encuentran en otros tipos de enfermedades inflamatorias y parecen ser un sello característico de la enfermedad con estos tipos de mutaciones UBA1.
Con base en las similitudes clínicas, identificaron 25 pacientes adicionales, todos varones, con mutaciones somáticas que afectan el codón metionina-41 de UBA1. En todos ellos, la enfermedad comenzó después de los 45 años y se presentó con síntomas como fiebre, inflamación de la piel, pulmones y cartílagos y problemas hematológicos como tromboembolismo, anemia y vacuolas en la médula ósea. El cuarenta por ciento de los pacientes ya falleció y la mayoría de ellos solo responde a dosis altas de esteroides o glucocorticoides.
El equipo decidió nombrar la nueva enfermedad, asociada a UBA1, VEXAS para síndrome: “Vacuolas, enzima E1, ligado al cromosoma X, Autoinflamatorio, Somático”. Para caracterizar aún más a VEXAS, el equipo examinó más de cerca los neutrófilos mutantes de los pacientes y descubrió que muchos de ellos estaban sufriendo muerte celular. Además, se descubrió que las células mieloides de los pacientes tenían vías inflamatorias altamente activadas, mientras que los linfocitos sin la mutación no las tenían. La enzima UBA1 generalmente se expresa como dos isoformas, una que reside en el citoplasma y la otra en el núcleo. El equipo encontró que las células mutantes de los pacientes habían perdido la isoforma citoplásmica y en su lugar, expresaban una nueva isoforma catalíticamente inactiva.
David B. Beck, MD, PhD, autor principal del estudio, dijo: “Las mutaciones somáticas pueden explicar una fracción significativa de las enfermedades inflamatorias de inicio en la edad adulta. Similar a la neoplasia, donde las mutaciones causan un crecimiento sostenido, en las enfermedades inflamatorias graves, las mutaciones somáticas pueden provocar una inflamación sostenida, como en VEXAS”. El estudio fue publicado el 27 de octubre de 2020 en la revista The New England Journal of Medicine.
Enlace relacionado:
Instituto Nacional de Investigación del Genoma Humano