Validan la secuenciación dirigida de próxima generación para el diagnóstico de las enfermedades de almacenamiento lisosomal
Por el equipo editorial de LabMedica en español
Actualizado el 04 May 2020
Los trastornos de almacenamiento lisosomal (LSD) son un grupo de más de 50 trastornos raros heredados, caracterizados por la acumulación de metabolitos específicos no degradados en los lisosomas. Este almacenamiento excesivo es comúnmente causado por una actividad deficiente o ausente de una de las muchas hidrolasas lisosómicas o, en algunos casos, por el déficit de otras proteínas lisosómicas no enzimáticas.Actualizado el 04 May 2020
En general, el enfoque de diagnóstico incluye una evaluación clínica exacta, que conduce a la formulación de una sospecha de que el paciente tiene una o más LSD. Esto es seguido por pruebas bioquímicas, destinadas a detectar los productos de almacenamiento en los fluidos corporales, cuyos resultados pueden orientar los análisis enzimáticos siguientes. Finalmente, si se detecta un déficit enzimático, se realiza un análisis genético del gen sospechoso.
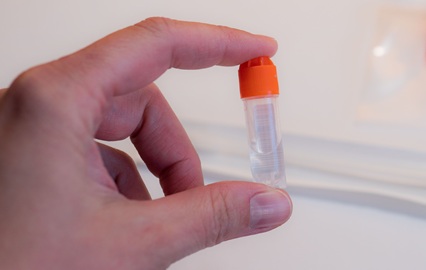
Imagen: El kit de análisis Invitrogen Qubit 1X dsDNA HS (Fotografía cortesía de Thermo Fisher Scientific).
Los científicos especializados en LSD de la Universidad de Padua (Padua, Italia) evaluaron un panel de secuenciación dirigida para las LSD, como una herramienta capaz de revertir potencialmente esta ruta de diagnóstico clásica. El panel incluye 50 genes de LSD y 230 secuencias intrónicas conservadas entre 33 mamíferos placentarios. Para la fase de validación, se analizaron 56 controles positivos, 13 pacientes con diagnóstico bioquímico y nueve pacientes no diagnosticados.
Los investigadores utilizaron la plataforma, Ion AmpliSeq (Thermo Fisher Scientific, Waltham, MA; EUA), para el diseño de un panel que incluía los genes seleccionados. La preparación de la biblioteca de ADN se realizó de acuerdo con el protocolo de preparación de la biblioteca Ion AmpliSeq de Thermo Fisher Scientific, en combinación con el kit de la biblioteca Ion AmpliSeq versión 2.0. Después de la cuantificación de ADN usando el kit de análisis Qubit dsDNA HS, las bibliotecas se construyeron a partir de 10 ng de cada muestra de ADN. El primer paso de la amplificación del objetivo se realizó mediante el uso de nuestros grupos de Panel de Sondas, AmpliSeq LSD. Luego se indexaron los amplicones usando el kit Ion Xpress Barcode Adapters y se purificaron usando cuentas magnéticas AMPure XP (Beckman Coulter, Inc., Brea, CA, EUA).
El equipo identificó variantes que causan enfermedades en el 66% de los alelos de control positivo y en el 62% de los pacientes con diagnóstico bioquímico. Tres pacientes no diagnosticados fueron diagnosticados. Ocho pacientes no diagnosticados por el panel fueron analizados por secuenciación completa del exoma: para dos de ellos, se identificaron las variantes causantes de la enfermedad. Cinco pacientes, no diagnosticados por los análisis de panel y del exoma, fueron investigados a través de la hibridación genómica comparativa de la matriz y uno de ellos fue diagnosticado. El análisis de fragmentos intrónicos conservados, realizado en casos no resueltos por el análisis de primer nivel, no evidenció variantes intrónicas candidatas.
Los autores concluyeron que la secuenciación dirigida es un método atractivo para implementar una estrategia de diagnóstico de rutina, dados sus bajos costos de secuenciación y su corto tiempo de secuenciación. Sin embargo, se debe garantizar una buena cobertura y, cuando no se alcanza, se debe realizar una validación por secuenciación de Sanger en el probando y en los padres como paso final, también para excluir la presencia de deleciones en casos de hallazgo de variantes homocigóticas. El estudio fue publicado en la edición de abril de 2020 de la revista Journal of Molecular Diagnostics.
Enlace relacionado:
Universidad de Padua
Beckman Coulter