Detectan poblaciones heterogéneas de células tumorales circulantes de melanoma
Por el equipo editorial de LabMedica en español
Actualizado el 03 Mar 2020
Las células tumorales circulantes (CTC) se pueden evaluar a través de una muestra de sangre mínimamente invasiva con utilidad potencial como biomarcador predictivo, pronóstico y farmacodinámico. La gran heterogeneidad de las CTC de melanoma ha dificultado su detección y aplicación clínica.Actualizado el 03 Mar 2020
Una forma nueva de detectar las células de melanoma que circulan en la sangre tiene el potencial de mejorar significativamente la monitorización de los pacientes con cáncer y guiar el tratamiento futuro. Se han comparado dos plataformas para el aislamiento y la purificación de células tumorales circulantes (CTC) de melanoma a partir de muestras de sangre de pacientes.

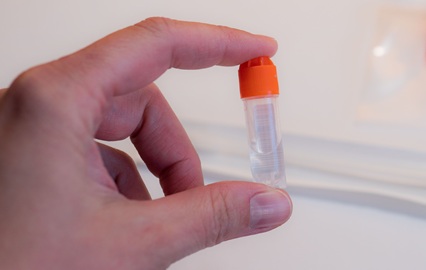
Imagen: La nueva plataforma ClearCell FX1 para detectar ADN tumoral circulante a partir de muestras de sangre (Fotografía cortesía de Explorea s.r.o.).
Un equipo internacional de científicos dirigido por los de la Universidad Edith Cowan (Perth, Australia) comparó dos dispositivos microfluídicos para la recuperación de células de melanoma circulante. La presencia de CTC en 43 muestras de sangre de pacientes con melanoma metastásico se evaluó mediante una combinación de inmunocitoquímica y análisis de transcripción de cinco genes por RT-PCR y 19 genes por PCR digital de gotitas (ddPCR), a través de la que se calculó una puntuación de CTC.
Se evaluó el ADN tumoral circulante (ADNc) de la misma muestra de sangre del paciente con la metodología de ddPCR dirigido a mutaciones específicas del tumor (Bio-Rad, Hércules, CA, EUA). Los dos dispositivos utilizados fueron el sistema de separación celular Parsortix (Angle, The Surrey Research Park, Reino Unido) y la plataforma ClearCell FX1 (Biolidics, Singapur).
El sistema de clasificación celular Parsortix utiliza casetes desechables microfluídicos para capturar y cosechar CTC en función de su naturaleza menos deformable y de mayor tamaño, en comparación con otros componentes sanguíneos. Las células capturadas se pueden fijar y colorear para la identificación y enumeración en casete o se pueden recuperar para la coloración externa y el análisis molecular con qPCR y otras técnicas. El sistema ClearCell FX1 es un dispositivo de biopsia líquida sin etiquetas que, según la firma, automatiza el aislamiento y enriquecimiento de CTC y ofrece dos protocolos de pureza diferentes. Después de lisar los glóbulos rojos en una muestra de sangre, la plataforma pasa la muestra a través de su biochip microfluídico CTChip FR1 de un solo uso para aislar las CTC de un fondo de glóbulos blancos (GB).
El equipo comparó muestras de sangre de 10 pacientes metastásicos. Usando inmunocoloración, los investigadores vieron que Parsortix producía, en promedio, un fondo GB dos veces menor que el producido por ClearCell. Detectaron CTC en el 30% de las muestras de pacientes con melanoma procesadas a través de Parsortix (rango de 1 a 13 CTC) y ClearCell (rango de 2 a 10 CTC). Mediante la RT-PCR, el grupo detectó con éxito al menos una transcripción de melanoma en 40% y 60% de las muestras enriquecidas por Parsortix y ClearCell, respectivamente. Los autores del estudio también encontraron que ClearCell detectó CTC en muestras que Parsortix no identificó y notaron que las fracciones enriquecidas con ClearCell también mostraron una abundancia ligeramente mayor de transcripciones detectadas en comparación con las muestras derivadas de Parsortix.
Al comparar las fracciones de CTC derivadas de 43 muestras de sangre de pacientes con melanoma, el equipo detectó CTC por inmunocitoquímica en 12 de las 43 muestras. Además, vieron que las CTC variaban en tamaño, desde 10,2 µm hasta 68,3 µm. El estudio fue publicado el 10 de febrero de 2020 en la revista British Journal of Cancer.
Enlace relacionado:
Universidad Edith Cowan
Bio-Rad
Angle
Biolidics