Biomarcador recién identificado diferencia los meningiomas potencialmente agresivos
Por el equipo editorial de LabMedica en español
Actualizado el 19 Nov 2019
La identificación de un biomarcador nuevo permitirá a los médicos diferenciar entre los meningiomas verdaderamente benignos y aquellos que eventualmente progresarán, crecerán rápidamente y se propagarán.Actualizado el 19 Nov 2019
Los meningiomas, que surgen de las membranas que rodean el cerebro y la médula espinal, son los tumores más comunes que surgen del sistema nervioso central. Los meningiomas se clasifican según su apariencia microscópica, tasa de crecimiento y tendencia a extenderse a otros tejidos. La mayoría de los meningiomas de grado 1 de la OMS tienen un pronóstico favorable. Sin embargo, algunos se vuelven clínicamente agresivos con recurrencia, invasión y resistencia a las terapias convencionales (grado 1.5; tumores recurrentes/progresivos grado 1 de la OMS que requieren tratamiento adicional dentro de los 10 años siguientes).
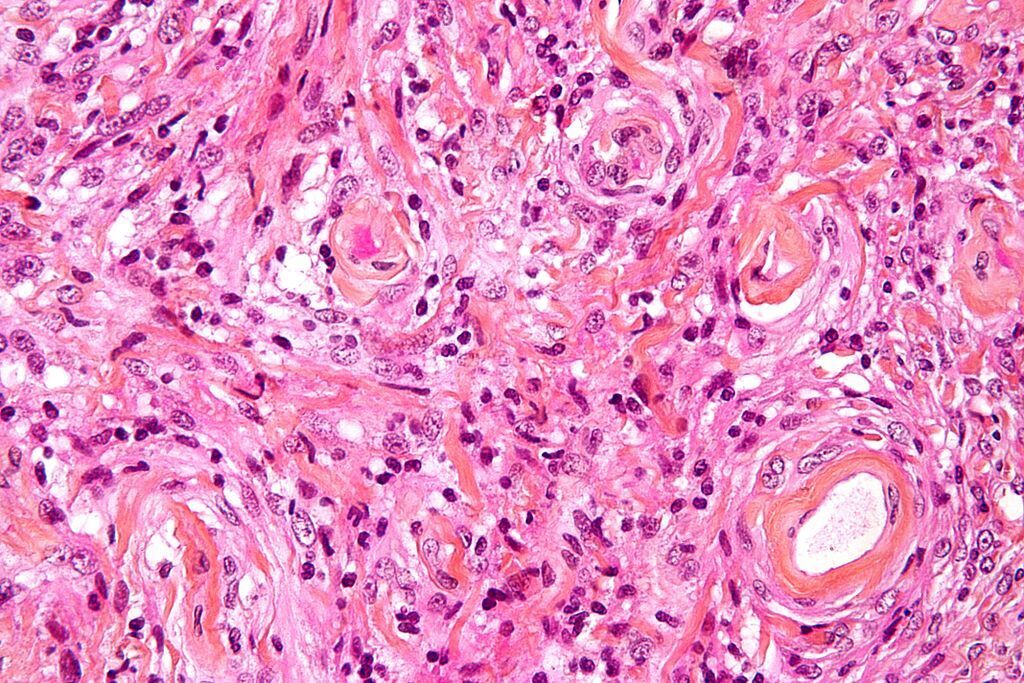
Imagen: Microfotografía de gran aumento de un meningioma que muestra los remolinos característicos (Fotografía cortesía de Wikimedia Commons).
Dado que no se conocen alteraciones genéticas reconocidas para distinguir los tumores de grado 1.5 de los de grado 1, los investigadores de la Facultad de Medicina de la Universidad de Washington (Seattle, EUA) examinaron la posibilidad de que las modificaciones en las proteínas fueran más probables en los tumores de grado 1.5.
Con este fin, utilizaron la fosfoproteómica basada en la espectroscopía de masas y la cinética de la matriz de chips de péptidos para comparar los tumores de grado 1 y 1.5.
La fosfoproteómica es una rama de la proteómica que identifica, cataloga y caracteriza las proteínas que contienen un grupo fosfato como una modificación postraduccional. La fosforilación es una modificación reversible clave que regula la función de las proteínas, la localización subcelular, la formación de complejos, la degradación de las proteínas y, por lo tanto, las redes de señalización celular. Se estima que entre el 30% y el 65% de todas las proteínas pueden estar fosforiladas, algunas muchas veces, lo que proporciona pistas sobre qué proteína o vía podría estar activada, dado que un cambio en el estado de fosforilación casi siempre refleja un cambio en la actividad proteica.
La quinómica es el estudio del quinoma, una descripción global de las quinasas y la señalización de las quinasas. Dado que las quinasas son responsables por numerosas vías de señalización en biología (tanto normales como en las enfermedades), la determinación de las quinasas pertinentes en un sistema biológico es de gran importancia.
Los resultados de la fosfoproteómica basada en espectrometría de masas revelaron fosforilación diferencial de la serina/treonina en 32 fosfopéptidos. El análisis quinómico por matriz de chips de péptidos identificó 10 fosfopéptidos, incluido un aumento del 360% en la fosforilación de la proteína del retinoblastoma 1 (RB1), en el grupo 1.5. La hiperfosforilación de Rb1 en el sitio S780 permitió diferenciar meningiomas de grado 1.5 en una cohorte independiente de 140 muestras y se asoció con una disminución de la supervivencia sin progresión/recurrencia.
“Los hemos designado grado 1.5 porque caen en algún lugar entre el grado 1 y el grado 2, pero hasta ahora no hemos tenido forma de saber qué tumores de grado 1 eran, de hecho, grado 1.5”, dijo el autor principal, el Dr. Manuel Ferreira, profesor asociado de cirugía neurológica en la Facultad de Medicina de la Universidad de Washington. “Se ven iguales bajo el microscopio y no hay marcadores genéticos claros u otros que los identifiquen. No sabemos qué causa que Rb1 se fosforile, y no sabemos qué efecto tiene sobre la fosforilación. Pero ahora podemos colorear el tejido de un paciente que tiene lo que parece ser un meningioma de grado 1 e identificar aquellos cuyos tumores pueden ser de grado 1.5, que requieren un seguimiento más cercano y tal vez un tratamiento adicional. Esperamos que esta proteína modificada no solo sirva como un biomarcador para identificar estos tumores, sino que también nos ayude a obtener información sobre las vías que impulsan su comportamiento”.
El estudio sobre el meningioma se publicó en la edición en línea del 15 de octubre de 2019 de la revista Clinical Cancer Research.
Enlace relacionado:
Facultad de Medicina de la Universidad de Washington